
科目: 来源: 题型:选择题
| A. | C4H8和C5H10 | B. | C3H8和C4H10 | ||
| C. | C2H4O2和C3H6O2 | D. | C6H5OH和C6H5CH2OH |
查看答案和解析>>
科目: 来源: 题型:实验题
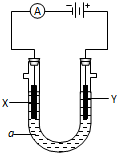 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连. 请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连. 请回答以下问题:查看答案和解析>>
科目: 来源: 题型:填空题
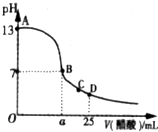 在25mL的氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,滴定曲线如图所示.
在25mL的氢氧化钠溶液中逐滴加入0.2mol/L醋酸溶液,滴定曲线如图所示.查看答案和解析>>
科目: 来源: 题型:多选题
| A. | Va>Vb时:c (CH3COOH)>c (CH3COO-)>c (K+) | |
| B. | Va=Vb时:c (CH3COOH)+c (H+)>c (OH-) | |
| C. | Va<Vb时:c (CH3COO-)>c (K+)>c (OH-)>c (H+) | |
| D. | Va与Vb任意比时:c (K+)+c (H+)=c (OH-)+c (CH3COO-) |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 硝酸银和氯化钠的混合溶液 | B. | 硫酸铜和硫酸钾的混合溶液 | ||
| C. | Na2CO3和NaOH混合溶液 | D. | CuCl2和HCl混合溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②③⑤⑧ | C. | ②③④⑦ | D. | 全部 |
查看答案和解析>>
科目: 来源: 题型:实验题
| 实验编号 | HA物质的量浓度(mol•L-1) | NaOH物质的量浓度(mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com