
科目: 来源: 题型:选择题
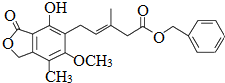 ,下列关于该化合物的说法不正确的是( )
,下列关于该化合物的说法不正确的是( )| A. | 该有机物的分子式为C23H24O6 | |
| B. | 1mol该化合物最多可以与9molH2发生加成反应 | |
| C. | 既可以使溴的四氯化碳溶液褪色,又可以使酸性KMnO4溶液褪色 | |
| D. | 既可以与FeCl3溶液发生显色反应,又可以与Na2CO3溶液反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2240mL | B. | 1008mL | C. | 3360mL | D. | 448mL |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 被还原的硝酸的物质的量为0.4mol | |
| B. | 测得生成沉淀的质量比原合金的质量增加20.4g | |
| C. | 原硝酸的浓度为1.6 mol/L | |
| D. | 合金中铝的质量为5.4g |
查看答案和解析>>
科目: 来源: 题型:解答题
| 酸 | 电离方程式 | 电离平衡常数K |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 |
| HClO | CHl0?ClO-+H+ | 3.0×10-8 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- | K1=4.4×10-7 K2=5.61×10-11 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++HPO43- | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{b-a}{V}$ mol•L-1 | B. | $\frac{2b-a}{V}$mol•L-1 | C. | $\frac{b-a}{V}$mol•L-1 | D. | $\frac{2(2b-a)}{V}$mol/L |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在蒸发食盐水时,边加热边用玻璃棒搅拌直至液体蒸干 | |
| B. | 鉴别Na2CO3与NaHCO3固体可用加热的方法 | |
| C. | 实验室制备氢氧化铁胶体时,向饱和氯化铁溶液中滴加氢氧化钠溶液 | |
| D. | 配制一定物质的量浓度的NaOH溶液,将NaOH固体放在容量瓶中加水溶解 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com