
科目: 来源: 题型:选择题

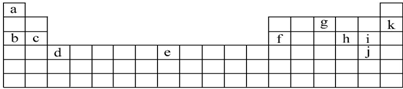
| A. | a、b、c的简单离子中,a的离子半径最大 | |
| B. | c、d、f最高价氧化物对应的水化物两两之间均可发生反应 | |
| C. | e的氢化物比f的氢化物的稳定性高 | |
| D. | a、e可形成一种新型无机非金属材料--高温结构陶瓷 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 6.4 | B. | 8 | C. | 3.2 | D. | 9.6 |
查看答案和解析>>
科目: 来源: 题型:解答题
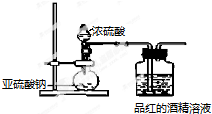
| 同浓度溶液 | SO${\;}_{3}^{2-}$ | HSO${\;}_{3}^{-}$ | H2SO3 | 褪色速度 |
| Na2SO3溶液 | 多 | 少 | 少 | 快 |
| NaHSO3溶液 | 较上面少 | 较上面多 | 较上面多 | 慢 |
查看答案和解析>>
科目: 来源: 题型:解答题
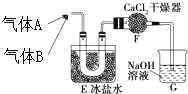 三种常见短周期元素组成的化合物甲,是有机合成中的重要试剂.常温下为黄色气体,具有刺鼻恶臭味,遇水和潮气分解.标况下测定其密度为2.92g/L.浓硝酸与浓盐酸混合制王水过程中会产生少量甲气体、黄绿色气体A和水.
三种常见短周期元素组成的化合物甲,是有机合成中的重要试剂.常温下为黄色气体,具有刺鼻恶臭味,遇水和潮气分解.标况下测定其密度为2.92g/L.浓硝酸与浓盐酸混合制王水过程中会产生少量甲气体、黄绿色气体A和水.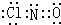 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 室温下,将等浓度等体积的NaHSO4和Ba(OH)2溶液混合并充分反应后的溶液中:c(Ba2+)+c(Na+)+c(H+)=c(SO42-)+c(OH-) | |
| B. | 向甲苯中滴加少量浓溴水并振荡静置,溶液分层且下层近无色,是因为发生了取代反应 | |
| C. | 可用稀盐酸酸化的BaCl2检验Na2SO3和Na2S2O3的混合液中是否混有Na2SO4 | |
| D. | 在与Al作用产生气体的溶液中一定不存在的离子组有:NO3-、Cl-、Na+、Mg2+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | I2、Br2、Cl2、F2 | B. | Li、Na、K、Rb | C. | F2、Cl2、Br2、I2 | D. | F-、Cl-、Br-、I- |
查看答案和解析>>
科目: 来源: 题型:解答题
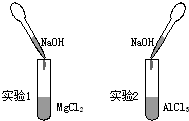 (1)已知反应:H2+Cl2$→_{400℃}^{CuO/CuCl_{2}}$2HCl,已知H-H键能为436kJ/mol,Cl-Cl键能为243kJ/mol,H-Cl键能为432kJ/mol.
(1)已知反应:H2+Cl2$→_{400℃}^{CuO/CuCl_{2}}$2HCl,已知H-H键能为436kJ/mol,Cl-Cl键能为243kJ/mol,H-Cl键能为432kJ/mol.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 明矾可以作净水剂 | |
| B. | 配制硫酸铁溶液时,先把硫酸铁晶体溶解在稀硫酸中,再加水稀释至所需浓度 | |
| C. | 加热稀氨水其溶液pH稍有变化 | |
| D. | 热的纯碱溶液可以去油污 |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com