
科目: 来源: 题型:选择题
| A. | 推广燃煤脱硫技术,减少SO2污染,同时把煤粉碎了再燃烧以提高煤的燃烧效率 | |
| B. | 开发太阳能、风能和氢能等能源代替化石燃料,有利于节约资源、保护环境 | |
| C. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 | |
| D. | 在汽车尾气处理器中使用新的催化剂,促使平衡2CO+2NO?2CO2+N2向正反应方向移动,减少污染物的排放 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1 mol•L-1•min-1 | B. | 0.2 mol•L-1•min-1 | ||
| C. | 0.3 mol•L-1•min-1 | D. | 0.6 mol•L-1•min-1 |
查看答案和解析>>
科目: 来源: 题型:解答题
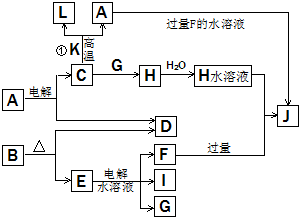 C、D、G、I均为短周期元素形成的单质,D、G、I为常见非金属气态单质.D的最外层电子数是次外层电子数的3倍,C、G同周期,且最外层电子数相差4,它们的简单离子电子层结构不同.相互间有如下转化关系:
C、D、G、I均为短周期元素形成的单质,D、G、I为常见非金属气态单质.D的最外层电子数是次外层电子数的3倍,C、G同周期,且最外层电子数相差4,它们的简单离子电子层结构不同.相互间有如下转化关系: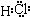 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ba2+、Na+、NO3-、I- | B. | H+、Ag+、NO3-、HCO3- | ||
| C. | Fe3+、Na+、S2-、Cl- | D. | Al3+、K+、Br-、SO42- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氧的摩尔质量是32g•mol-1 | B. | 硫酸的摩尔质量是98 g | ||
| C. | CO2的相对分子质量是44 g | D. | CO32-摩尔质量是60 g•mol-1 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验题
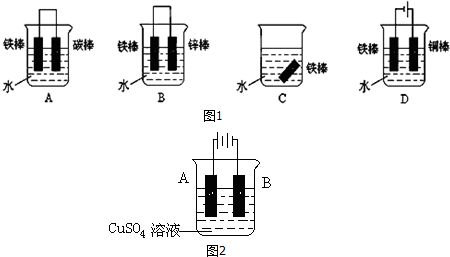
 Ⅰ.按图装置进行实验,并回答下列问题.
Ⅰ.按图装置进行实验,并回答下列问题. Ⅱ.(1)电工经常说的一句口头禅:“铜接铝,瞎糊弄”,所以电工操作上规定不能把铜导线与铝导线连接在一起使用,说明原因:铜与铝连接会构成原电池,其中铝为原电池的负极,铜为原电池的正极.构成原电池后,铝的腐蚀速度大大加快,电阻增大,放热增多,时间长了,有可能引发火灾.
Ⅱ.(1)电工经常说的一句口头禅:“铜接铝,瞎糊弄”,所以电工操作上规定不能把铜导线与铝导线连接在一起使用,说明原因:铜与铝连接会构成原电池,其中铝为原电池的负极,铜为原电池的正极.构成原电池后,铝的腐蚀速度大大加快,电阻增大,放热增多,时间长了,有可能引发火灾.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe(NO3)x中的x为2 | |
| B. | 稀HNO3在反应中只表现氧化性 | |
| C. | 反应中每还原0.4 mol氧化剂,就有1.2 mol电子被转移 | |
| D. | 磁性氧化铁中的铁元素全部被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com