
科目: 来源: 题型:计算题
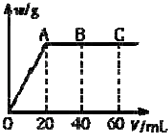 有H2SO4和HCl 的混合溶液20mL,加入0.025mol•L-1 Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C 点混合液pH=7).
有H2SO4和HCl 的混合溶液20mL,加入0.025mol•L-1 Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C 点混合液pH=7).查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 反应物和生成物都是非极性分子 | |
| B. | 0.5molHCHO 含有1molσ键 | |
| C. | HCHO、CO2分子中中心原子杂化类型相 | |
| D. | 液态水中只存在一种作用力同 |
查看答案和解析>>
科目: 来源: 题型:选择题
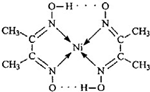 .对该物质的分析判断正确的是( )
.对该物质的分析判断正确的是( )| A. | 该物质是中不存在σ键 | |
| B. | 该物质的分子中只含有共价键、配位键两种作用力 | |
| C. | 该物质是一种配合物,其中N 原子为配位体 | |
| D. | 该物质中C、N、O 原子存在孤对电子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | W、Y、Z 的电负性大小顺序一定是Z>Y>W | |
| B. | Z 的氢化物分之间存在氢键 | |
| C. | Y、Z 形成的分子的中心原子可能采用sp3杂化 | |
| D. | WY2分子中σ键与π键的数目之比是2:1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
查看答案和解析>>
科目: 来源: 题型:推断题
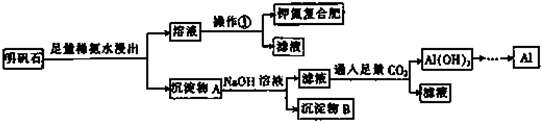
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 欲配制1.00 L 1.00 mol•L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 | |
| B. | 将80 g SO3溶于水并配成1 L溶液,溶质的物质的量浓度为1 mol•L-1 | |
| C. | 10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% | |
| D. | 1 mol•L-1 NaCl溶液含有NA个Na+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 热稳定性:HF>H2O>NH3>CH4 | |
| B. | 离子半径:S2->K+>Na+>Al3+ | |
| C. | 碱性:Mg(OH)2<KOH<CsOH | |
| D. | 给出质子的能力:H3PO4<H2SO4<HClO |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②③ | B. | ①③ | C. | ① | D. | ①④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com