
科目: 来源: 题型:选择题
| A | B | C | D | |
| 阳极 | 白 | 红 | 蓝 | 蓝 |
| 阴极 | 蓝 | 蓝 | 红 | 蓝 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| 阳极 | 阴极 | 溶液甲 | 物质乙 |
| A.Pt | Pt | NaOH | NaOH固体 |
| B.铜 | 铁 | CuSO4 | CuO |
| C.C | Pt | NaCl | 盐酸 |
| D.Pt | Pt | H2SO4 | H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
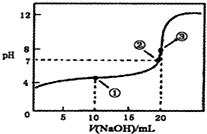
| A. | ①处水的电离程度大于②处水的电离程度 | |
| B. | ②处加入的NaOH溶液恰好将CH3COOH中和 | |
| C. | ③处所示溶液:c(N+)<c(CH3COO-) | |
| D. | 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向稀的Na2CO3和NaHCO3溶液中加入CaCl2溶液均有白色沉淀产生 | |
| B. | 向Al2(SO4)3溶液中逐滴滴入NaOH溶液与向NaOH溶液中逐滴滴入Al2(SO4)3溶液,产生的现象相同 | |
| C. | 等质量的Al分别与过量的NaOH、HCl溶液反应,NaOH溶液中放出的H2多 | |
| D. | 分别向Na2CO3和NaHCO3溶液中滴加澄清石灰水,都能生成白色沉淀 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 塑料奶瓶比玻璃奶瓶更有利于健康,且更加经久耐用 | |
| B. | SO2可以用来漂白纸浆,也可以用来漂白银耳等食品 | |
| C. | 家中做卫生保洁时,不可将漂白粉与洁厕精(含浓盐酸)混合使用 | |
| D. | 用K2FeO4取代Cl2处理饮用水,可杀菌消毒,但不能沉降水中的悬浮物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定条件下,当N2的生成速率与N2的分解速率相等时,该反应处于平衡状态 | |
| B. | 取1mol N2和3mol H2放在密闭容器内反应达平衡时,生成2 mol NH3 | |
| C. | 一定条件下反应达到平衡,再充入N2,则正反应速率增大,逆反应速率减小 | |
| D. | 一定条件下反应达到平衡,若升高温度,反应速率增大,平衡向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com