
科目: 来源: 题型:解答题
| 一溴代二甲苯 | 234℃ | 206℃ | 213.8℃ | 204℃ | 214.5℃ | 205 |
| 对应的二甲苯 | -13℃ | -54℃ | -27℃ | -54℃ | -27℃ | -54℃ |

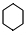 .
. (填任一种).
(填任一种).查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验题
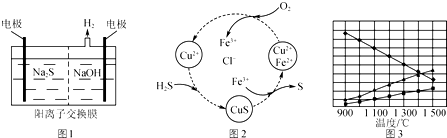
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在一个基态多电子的原子中,不可能有两个能量完全相同的电子 | |
| B. | M层全充满而N层为4s2的原子与核外电子排布式为1s22s22p63s23p63d64s2的原子位于同一族 | |
| C. | 如果某一基态原子3p能级上仅有2个电子,它们的自旋状态必然相同 | |
| D. | 价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
查看答案和解析>>
科目: 来源: 题型:推断题
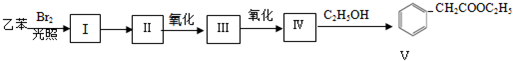
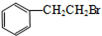 .
. .
.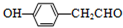 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com