
科目: 来源: 题型:选择题
| A. | 150mL1mol•L-1NaCl溶液 | B. | 100mL2mol•L-1KCl溶液 | ||
| C. | 75mL0.5mol•L-1CaCl2溶液 | D. | 75mL1mol•L-1AlCl3溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
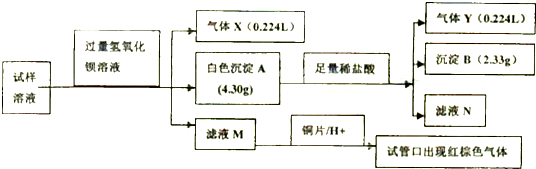
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 金属钠可以保存在煤油或酒精中,防止在空气中变质 | |
| B. | 钠是强氧化剂 | |
| C. | 钠与熔融的四氣化钛反应可制取钛 | |
| D. | 实验时用剩的钠块不应放回原试剂瓶 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | MgSO4、NaNO3、KNO3、 |
| 第二次 | Mg (NO3)2、KNO3、Na2SO4 |
| 第三次 | Mg (NO3)2、Ba(NO3)2、Na2SO4 |
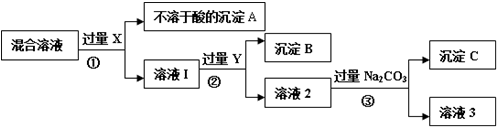
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 3:2 | B. | 1:3 | C. | 1:8 | D. | 2:5 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③④ | B. | ③④⑥ | C. | ①②④ | D. | ①③④⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 16gCH4含有共价键数为4NA | |
| B. | 1mol甲基中含有电子数为10NA | |
| C. | 7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA | |
| D. | 1molC3H8分子中共价键总数为8NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com