
科目: 来源: 题型:选择题
| A. | K+、Na+、MnO4-、NO3- | B. | K+、Na+、Cl-、NO3- | ||
| C. | NH4+、AlO2-、Na+、CH3COO- | D. | Fe3+、S2-、Al3+、HCO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 同主族金属的原子半径越大熔点越高 | |
| B. | 稀有气体原子序数越大沸点越高 | |
| C. | 同周期元素的原子半径越小越易失去电子 | |
| D. | 在晶体中只要有阳离子就一定有阴离子 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯气有氧化性,作用于正常细胞而癌化 | |
| B. | 氯水中的次氯酸具有杀菌性,氧化了正常细胞,异化为癌细胞 | |
| C. | 氯气有毒,杀死正常细胞,不杀灭癌细胞 | |
| D. | 氯气作用于水中有机物,生成有机氯化合物而致癌 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 通入少量 HCl 气体 | B. | 加入少量 NaOH 固体 | ||
| C. | 加入少量 H2O | D. | 适当升高温度 |
查看答案和解析>>
科目: 来源: 题型:推断题
 甲、乙、丙、丁、戊为原子序数依次增大的短周期元素.甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和.甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1 mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z的水溶液反应生成盐;丙、戊可组成化合物M.
甲、乙、丙、丁、戊为原子序数依次增大的短周期元素.甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和.甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1 mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z的水溶液反应生成盐;丙、戊可组成化合物M.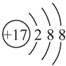 .
.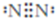 .
.查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 向待测溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- | |
| B. | 向待测溶液中逐滴加入氢氧化钠溶液,开始有白色沉淀生成,继续滴加氢氧化钠溶液到过量,沉淀逐渐溶解,一定有 Al3+ | |
| C. | 向待测溶液中先滴加盐酸酸化未出现沉淀,再加入 BaCl2 溶液有白色沉淀产生,一定有SO42- | |
| D. | 向待测溶液中滴加 NaOH 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,一定有NH4+ |
查看答案和解析>>
科目: 来源: 题型:实验题
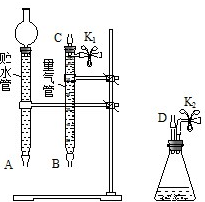 某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.
某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.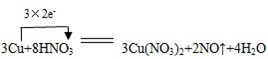 .
.| 实验编号 | 稀硝酸的浓度 /(mol/L) | 稀硝酸的体积 /mL | 温度 /℃ | 时间 /min | 收集气体的体积/mL |
| ① | a | V | 25 | t1 | V1 |
| ② | V | ||||
| ③ | V |
查看答案和解析>>
科目: 来源: 题型:推断题
| 元素代号 | 相关信息 |
| T | T 的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X | X 的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期金属元素中,Y 的简单离子半径最小 |
| Z | T、X、Z 组成的 36 电子的化合物 A 是家用消毒剂的主要成分 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com