
科目: 来源: 题型:选择题
| A. | KCl、Na2SO4 | B. | KCl、Na2SO4、NaCl | ||
| C. | NaCl、Na2SO4、K2SO4 | D. | KCl、K2SO4、Na2SO4 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 水的沸点;蒸发水所需热量 | |
| B. | 水的密度;水中通入足量CO2后溶液的pH | |
| C. | 水的体积;电解水所消耗的电量 | |
| D. | 水的物质的量;水的摩尔质量 |
查看答案和解析>>
科目: 来源: 题型:解答题
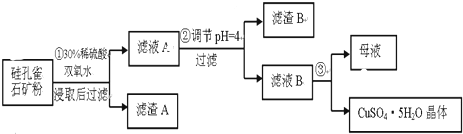
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
查看答案和解析>>
科目: 来源: 题型:解答题

 $\stackrel{H_{2}O/H+}{→}$
$\stackrel{H_{2}O/H+}{→}$
 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$ (-NH2易被氧化)
(-NH2易被氧化) .
. .
.
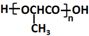 的合成路线:
的合成路线: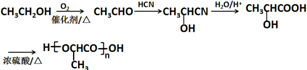 .(无机试剂任选)合成路线示例:CH≡CH$→_{催化剂/△}^{H_{2}}$CH2=CH2$→_{催化剂/△}^{HCl}$CH3CH2Cl.
.(无机试剂任选)合成路线示例:CH≡CH$→_{催化剂/△}^{H_{2}}$CH2=CH2$→_{催化剂/△}^{HCl}$CH3CH2Cl.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等 | |
| B. | 通信光缆的主要成分是晶体Si,太阳能电池的材料主要是SiO2 | |
| C. | 高锰酸钾溶液、酒精、双氧水都能杀菌消毒,都利用了强氧化性 | |
| D. | 氨很容易液化,液氨气化吸收大量的热,所以液氨常用作致冷剂 |
查看答案和解析>>
科目: 来源: 题型:解答题
 氮元素的氢化物和氧化物在工业生产和防建设中都有广泛的应用.请回答下列问题:
氮元素的氢化物和氧化物在工业生产和防建设中都有广泛的应用.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1L0.1mol/L的NaF溶液中,含F-的数目小于0.1NA | |
| B. | 电解食盐水产生2gH2时转移的电子数为2NA | |
| C. | 标况下22.4L溴所含分子数目为2NA | |
| D. | 同温同压下,原子数均为NA的氢气和氦气具有相同的体积 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X2YZ3 | B. | XYZ2 | C. | X3YZ4 | D. | XYZ3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①④⑤⑥ | B. | ①②③⑤ | C. | ②③④⑥ | D. | 以上全部 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com