
科目: 来源: 题型:实验题
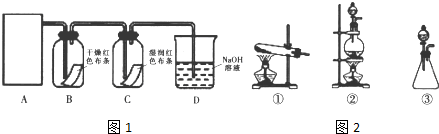
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 再通入$\frac{W}{10}$g氯化氢 | B. | B、蒸发浓缩成$\frac{W}{2}$g | ||
| C. | 蒸发掉溶剂的一半 | D. | 再加入2Wg25%盐酸 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | NaHSO4固体是离子晶体 | |
| B. | NaHSO4晶体中阳离子和阴离子的个数是2:1 | |
| C. | NaHSO4晶体熔化时破坏的是离子键和共价键 | |
| D. | NaHSO4固体溶于水时既破坏离子键又破坏共价键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯化氢是白色有刺激性气味的气体 | |
| B. | 氯化氢具有强酸性 | |
| C. | 氯化氢能使干燥的蓝色石蕊试纸变红 | |
| D. | 氯化氢极易溶于水 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 都是银白色的质软金属,密度都很小 | |
| B. | 单质在空气中燃烧生成的都是过氧化物 | |
| C. | 碱金属单质与水剧烈反应生成碱和H2 | |
| D. | 单质熔沸点随着原子序数的增加而升高 |
查看答案和解析>>
科目: 来源: 题型:解答题
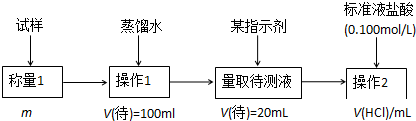
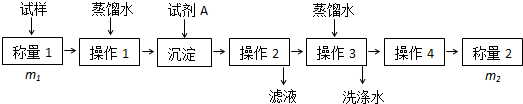
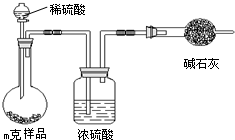
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2CO3 | B. | NaHCO3 | C. | Na2CO3和NaHCO3 | D. | Na2SO4 |
查看答案和解析>>
科目: 来源: 题型:选择题
| X | R | Y | |
| Z | W |
| A. | Y元素的最高价氧化物的水化物是含氧酸中酸性最强的 | |
| B. | W和R只能形成一种化合物WR3,且为酸性氧化物 | |
| C. | X的最高价含氧酸与它的简单气态氢化物发生氧化还原反应 | |
| D. | Z与R形成的化合物ZR2是生产光纤制品的基本原料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com