
科目: 来源: 题型:解答题
 ,常用于汽水、糖果的添加剂.
,常用于汽水、糖果的添加剂.查看答案和解析>>
科目: 来源: 题型:解答题
 ,
, ,
, ,
,查看答案和解析>>
科目: 来源: 题型:填空题
 ⑨淀粉和纤维素
⑨淀粉和纤维素查看答案和解析>>
科目: 来源: 题型:解答题
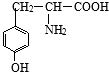 有一种结构简式如图的有机物,请回答下列问题:
有一种结构简式如图的有机物,请回答下列问题: +2NaOH→
+2NaOH→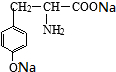 +2H2O.
+2H2O.查看答案和解析>>
科目: 来源: 题型:解答题
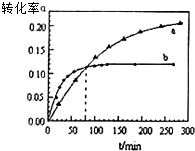 丙酮(CH3COCH3)可作为合成聚异戊二烯橡胶,环氧树脂等物质的重要原料,丙酮在某溶剂里在催化剂作用下发生反应:2CH3COCH3(aq)?CH3COCH2COH(CH3)2(aq).回答下列问题
丙酮(CH3COCH3)可作为合成聚异戊二烯橡胶,环氧树脂等物质的重要原料,丙酮在某溶剂里在催化剂作用下发生反应:2CH3COCH3(aq)?CH3COCH2COH(CH3)2(aq).回答下列问题查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 18gNH4+中含有的电子数为11NA | |
| B. | 12g石墨中含有的共价键数为1.5NA | |
| C. | 标准状况下,22.4LNO2和CO2混合物中含有原子总数为3NA | |
| D. | 1 mol Na与足量O2反应,生成 Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 高纯度的硅晶体广泛用于制造光导纤维材料 | |
| B. | 燃烧化石燃料产生的废气中含有 SO2,会造成大气污染,使雨水 pH=5.6形成酸雨 | |
| C. | “春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是蛋白质和烃 | |
| D. | 海轮外壳上镶入铜块,可以延缓船体腐蚀 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com