
科目: 来源: 题型:选择题
| A. | 乙醇和乙二醇互为同系物 | |
| B. | 异丙苯(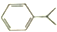 )分子中碳原子可能都处于同一平面 )分子中碳原子可能都处于同一平面 | |
| C. | 按系统命名法,化合物(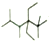 )的名称是2,3,5,5一四甲基一4,4一二乙基己烷 )的名称是2,3,5,5一四甲基一4,4一二乙基己烷 | |
| D. | 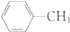 的一溴代物和 的一溴代物和 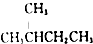 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加铝粉能产生大量H2的溶液中:Na+、NH4+、NO3-、Cl- | |
| B. | 使甲基橙变红色的溶液中:K+、NH4+、HCO3-、Cl- | |
| C. | 由c(H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO3- | |
| D. | 水电离出的c(H+)=10-12mol•L-1的溶液中:Mg2+、Cu2+、SO42-、K+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 过氧化钠与水反应时,生成0.1molO2转移的电子数为0.2NA | |
| B. | 4.48L氨气分子中含0.6NA个N-H键 | |
| C. | 100ml0.2mol•L-1的FeCl3溶液中,含Fe3+数为0.02NA | |
| D. | 密闭容器中2molNO与1molO2充分反映,产物的分子数为2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 凡含有添加剂的食物对人体健康均有害,不宜食用 | |
| B. | 火力发电中,燃烧是使化学能转换为电能的关键 | |
| C. | 塑胶跑道的主要成分聚氨酯属于有机高分子化合物 | |
| D. | 原子经济性反应是绿色化学的重要内容 |
查看答案和解析>>
科目: 来源: 题型:解答题


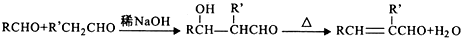
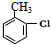 ,H→I两步反应的反应类型加成反应、消去反应.
,H→I两步反应的反应类型加成反应、消去反应.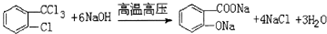 ,E→F
,E→F

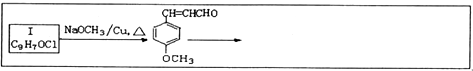
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验题

查看答案和解析>>
科目: 来源: 题型:推断题
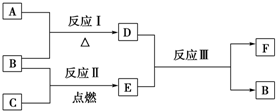
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | K+、CO32-、S2-、Cl- | B. | NO3-、Br-、Na+、NH4+ | ||
| C. | Na+、K+、Cl-、HS- | D. | Na+、NO3-、Fe3+、SO4- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com