
科目: 来源: 题型:解答题
 H2AsO3-+OH(用离子方程式表示),该溶液中c(H2AsO3-)>c(AsO33-)(填”>”、“<”或“=”).
H2AsO3-+OH(用离子方程式表示),该溶液中c(H2AsO3-)>c(AsO33-)(填”>”、“<”或“=”).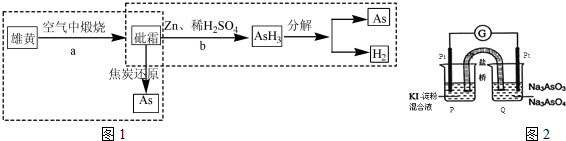
查看答案和解析>>
科目: 来源: 题型:解答题
 ;
; ;
; 和a个-CH3,其余为-OH,则-OH 的个数为m+2-a
和a个-CH3,其余为-OH,则-OH 的个数为m+2-a查看答案和解析>>
科目: 来源: 题型:解答题
 此烃名称为4-甲基-1-戊炔.
此烃名称为4-甲基-1-戊炔. 的烃可命名为1-甲基-3-乙基苯.
的烃可命名为1-甲基-3-乙基苯. 的烃可命名为:2,4-二甲基-3-乙基戊烷.
的烃可命名为:2,4-二甲基-3-乙基戊烷. 的键线式:
的键线式: .
. 的键线式:
的键线式: .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ⅠA族和ⅥA族元素形成的原子个数比为1:1、电子总数为38的化合物,是含共价键的离子化合物 | |
| B. | 在SiO2晶体中,1个硅原子和2个氧原子形成2个共价键 | |
| C. | HI的相对分子质量比HF大,所以HI的沸点比HF高 | |
| D. | H与D、16O与18O互为同位素;H216O、D216O、H218O、D216O互为同素异形体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | PH<7的溶液:Cu2+、Na+、Mg2+、NO3- | |
| B. | 滴加酚酞试液显红色的溶液:Fe3+、NH4+、Cl-、NO3- | |
| C. | 所含溶质为NaOH的溶液中:K+、SO42-、NO3-、H+ | |
| D. | 在碱性溶液:K+、HCO3-、Br-、Ba2+ |
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 氯化氢能使湿润的蓝色石蕊试纸变为红色,是因为HCl分子中含有H+ | |
| B. | 氯化氢极易溶于水,常温常压下1体积水可溶解500体积HCl | |
| C. | 氯化氢可以用向上排空气法收集 | |
| D. | 氯化氢和盐酸的化学式都是HCl |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 阴极呈无色,阳极呈红色 | B. | 正极呈红色,负极呈无色 | ||
| C. | 阳极呈无色,阴极呈红色 | D. | 负极呈红色,正极呈无色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com