
科目: 来源: 题型:
某学生欲用已知物质的量浓度的HCl测定未知浓度的NaOH溶液,将HCl置于滴定管,氢氧化钠溶液置于锥形瓶,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定未知浓度的NaOH溶液,滴定到终点时锥形瓶中颜色变化为 。
(2)下列操作中可能无法会怎样影响所测NaOH溶液浓度(填偏大.偏小或不影响)
A.酸式滴定管未用标准浓度的HCl润洗就直接注入标准盐酸
B.读数时,开始平视,结束时俯视液面
(3)某学生根据3次实验记录有关数据如下:
| 滴定次数 | 待测NaOH溶液体积(mL) | 0.1000mol/L HCl溶液的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
请选择合理的数据计算NaOH溶液的物质的量浓度:c(NaOH)=________________。
查看答案和解析>>
科目: 来源: 题型:
在25℃时,用石墨电极电解![]() ,
,![]() 溶液。5min后,在一个石墨电极上有6.4g Cu生成。试回答:
溶液。5min后,在一个石墨电极上有6.4g Cu生成。试回答:
(1)转移电子的物质的量,得到![]() 的体积(标准状况),溶液的
的体积(标准状况),溶液的![]() ?
?
2)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差多少?电解液的![]() 是否变化? (相对原子质量 Cu:64)
是否变化? (相对原子质量 Cu:64)
查看答案和解析>>
科目: 来源: 题型:
在一定温度下(已知在该温度下,容器内所有物质均为气态),10 L密闭容器中加入5 mol SO2.4 mol O2,经10 min后反应达平衡时有2 mol SO2发生了反应。试计算:
(1)用SO2表示该反应的反应速率;
(2)O2的转化率;
(3)该温度下的平衡常数K(保留三位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
NA为阿伏伽德罗常数,下列叙述错误的是( )
A.18gH2O中含的质子数为10NA
B.12g 金刚石含有的共价键数为4NA
C.46gNO2和N2O4混合气体中含有原子总数为3NA
D.1 mol Na 与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏伽德罗常数,下列叙述正确的是( )
A.24g镁的原子量最外层电子数为NA
B.1L0.1mol·L-1乙酸溶液中H+数为0.1NA
C.1mol甲烷分子所含质子数为10NA
D.标准状况下,22.4L乙醇的分子数为NA
查看答案和解析>>
科目: 来源: 题型:
某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
A.K+、Na+、HCO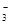 、NO
、NO![]() B.Na+、SO
B.Na+、SO![]() 、Cl—、ClO—
、Cl—、ClO—
C.H+、Mg2+、SO![]() 、NO
、NO![]() D.Ag+、K+、NO
D.Ag+、K+、NO![]() 、Na+
、Na+
查看答案和解析>>
科目: 来源: 题型:
水作为还原剂的反应是:( )
A、2Na + 2H2O=2NaOH+ H2↑ B、SO3 + H2O=H2SO4
C、2F2 + 2H2O=4HF + O2↑ D、2H2 + O2 2H2O
查看答案和解析>>
科目: 来源: 题型:
能正确表示下列化学反应的离子方程式是( )
A、氢氧化钡溶液与稀硫酸的反应:OH-+H+=H2O
B、澄清的石灰水与稀盐酸反应: Ca(OH)2+2H+=Ca2++2H2O
C、铜丝插入硫酸铁溶液中: 2Fe3+ + Cu = Cu2+ + 2Fe2+
D、碳酸钙溶于稀盐酸中: CO32- + 2H+=H2O + CO2↑
查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:rX>rY>rZ>rW>rQ
C.离子Y2-和Z 3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目: 来源: 题型:
相同物质的量的铝箔分别与足量的稀盐酸、浓氢氧化钠溶液反应,待完全反应后,消耗的盐酸和氢氧化钠的物质的量之比为( )
A、2∶3 B、3∶1 C、1∶1 D、1∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com