
科目: 来源: 题型:
下列叙述不正确的是( )
A.向澄清石灰水中通入CO2产生白色沉淀,再通入过量CO2,沉淀消失
B.向AlCl3溶液中滴加NaOH溶液,产生白色沉淀,再加入过量NaOH溶液,沉淀消失
C.向AgNO3溶液中滴加氨水,产生白色沉淀,再加入过量氨水,沉淀消失
D.向Na2SiO3溶液中滴加盐酸,产生白色沉淀,再加入过量盐酸,沉淀消失
查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z在元素周期表中的位置如右下图所示,下列说法正确的是( )
A.X、Y、Z三种元素中,X的非金属性最强
B.Y的原子半径比Z小
C.Y的最高正化合价为+7
D.Y的氢化物的稳定性比Z的氢化物弱
查看答案和解析>>
科目: 来源: 题型:
取某铁的氧化物样品,用140mL 5 mol/L盐酸恰好使其完全溶解,所得溶液还能吸收标准状况下0.56 L氯气,使其中的Fe2+ 完全转化为 Fe3+,该样品中可能的化学式是( )
A.Fe3O4 B.Fe4O5 C.Fe5O6 D.Fe5O7
查看答案和解析>>
科目: 来源: 题型:
选用合适的试剂,采用适当的操作进行除杂实验(下表括号中物质为杂质)。请在下表中写出合适的除杂试剂的名称或化学式,并写出主要反应的离子方程式。
| 序号 | 实验内容 | 除杂试剂 (名称或化学式) | 主要反应的离子方程式 |
| 1 | Cu(Fe) |
|
|
| 2 | FeCl2 (FeCl3) |
|
|
| 3 | Mg(Al) |
|
|
查看答案和解析>>
科目: 来源: 题型:
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最高正化合价与最低负化合价的绝对值相等;M是地壳中含量仅次于氧元素的非金属元素;L的最简单气态氢化物甲能使湿润的红色石蕊试纸变蓝。
(1)M的原子结构示意图为________ ;元素R在周期表中位于第_____周期,第_____族, 元素T最高价氧化物对应水化物化学式是________。
(2)写出J和氧形成的一种酸性氧化物的电子式____________,含有共价键是______(填极性键或非极性键)。
(3)写出能说明T非金属性比R强的反应的化学方程式___________________________
(4)在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为______________________________________
(5)0.2mol由M形成的气态氢化物在O2中完全燃烧,生成一种固体和液态水,298K时放出热量a kJ 。 该反应的热化学方程式为_____________________________________________
查看答案和解析>>
科目: 来源: 题型:
A~K为中学化学常见的物质,它们之间的转化关系如下图,部分生成物和反应条件等省略。已知C、D是由元素X、Y、Z中的两种组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色气体且不能燃烧,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板。请回答下列问题:
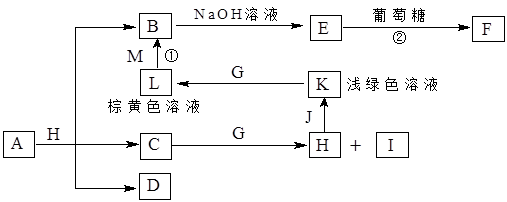
1)写出A的化学式______________。
(2)比较Y与Z的原子半径大小:_________>_______(填写元素符号)。
(3)检验L溶液中金属阳离子的方法是__________________________________。
(4)已知F溶于稀硝酸,溶液变成蓝色,放出无色气体。请写出该反应的化学方程式
________________________________________________________
查看答案和解析>>
科目: 来源: 题型:
聚合硫酸铁又称聚铁,化学式![]() ,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:
,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:
(1)验证固体W焙烧后产生的气体含有SO2的方法是 _________________________
(2)实验室制备,收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器口顺序为a _____
_____![]() _____
_____![]() _____
_____![]() _____
_____![]() f(填接口字母)。装置D的作用是__________。
f(填接口字母)。装置D的作用是__________。
(3)制备绿矾时,向溶液X中加入过量________,充分反应后,经过滤操作得溶液Y,再经浓缩,结晶等步骤得到绿矾。
(4)若取m g制得的绿矾样品溶于水加入足量BaCl2溶液充分反应,过滤、洗涤、干燥,最终得n g BaSO4沉淀,则该绿矾含FeSO4·7H2O的质量分数为________(用含m、n代数式表示)。
(5)溶液Z的pH影响聚铁中铁的质量分数,要测定溶液Z的pH,除了需要溶液Z、pH试纸、表面皿、玻璃棒等仪器、药品外,还需要的一种仪器或药品是_____________________。若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏_____(大或小) 。
查看答案和解析>>
科目: 来源: 题型:
下列说法中,错误的是
A.蛋白质、淀粉、纤维素水解的最终产物都是纯净物
B.误服重金属盐,立即服用牛奶或豆浆可解毒
C.油脂、乙酸乙酯都属于酯类,但不是同系物
D.苯和乙烯都能发生加成反应
查看答案和解析>>
科目: 来源: 题型:
NA为阿伏加德罗常数的数值,下列说法正确的是
A.标准状况下22.4 LCl2与足量NaOH溶液反应生成NaCl和NaClO,转移电子数为NA
B.电解精炼铜时转移了6.02×1023个电子,阳极溶解32 g铜
C.一定量的SO2溶于水后形成pH为2的水溶液,其中H+ 的数目为0.01NA
D.含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1×6.02×1023
查看答案和解析>>
科目: 来源: 题型:
下图装置或操作正确的是
A.用装置①量取15.00ml的NaOH溶液
B.用装置②制备Cl2
C.用装置③高温煅烧CaCO3固体
D.关闭活塞a,从b处加水,以检查装置④的气密性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com