
科目: 来源: 题型:
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法正确的是
( )
A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
B.原溶液中一定含有SO42-和Na+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D.反应最后形成的溶液中含有的溶质为Na2SO4
查看答案和解析>>
科目: 来源: 题型:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2OO 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是 ( )
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O
C.放电时每转移3mol电子,正极有1molK2FeO4被还原
D.放电时正极附近溶液的碱性减弱
查看答案和解析>>
科目: 来源: 题型:
某温度时,AgCl (s)Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是 ( )
A.加入AgNO3可以使溶液由c点变到d点
B.加入固体NaCl则AgCl的溶解度减小,Ksp也减小
C.d点有AgCl沉淀生成
D.c点对应的Ksp小于a点对应的Ksp
查看答案和解析>>
科目: 来源: 题型:
一定量的Fe和Fe2O3混合物投入2 mol/L 250ml的HNO3溶液中,反应完全后,无固体剩余,生成1.12L NO气体(标况),再向反应后溶液中加入1 mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是( )
A.450ml B.500ml C.400ml D.无法确定
查看答案和解析>>
科目: 来源: 题型:
四种短周期元素A、B、C、D的性质或结构信息如下:
信息① 原子半径大小:A>B>C>D
信息② 四种元素之间形成的某三种分子的比例模型及部分性质:
请根据上述信息回答下列问题。
(1)B元素在周期表中的位置 ,请写出BC2分子的电子式 。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂。E单质与甲反应有化合物X生成。请写出以下两个反应的离子方程式。
①A元素的单质与物质甲发生的反应 。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生的反应 。
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液。滴加过程中的现象是:
①浅绿色溶液变成深棕黄色,②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,并放出较多热量,继续滴加溶液,静置一段时间,③试管中出现红褐色。向其中再滴入稀硫酸,红褐色变为黄色。请用化学方程式或离子方程式①、②、③中加点的字。
① ② ③ 。
查看答案和解析>>
科目: 来源: 题型:
照相用的废定影液中含有Na+、[Ag(S2O3)2]3-、Br-等离子。某研究性学习小组拟通过下列实验程序,对某照相公司的废定影液进行实验处理,回收其中的银和溴。
(已知:4H++2 [Ag(S2O3)2]3-= Ag2S↓+3S↓+3SO2↑+SO42-+2H2O)
⑴操作Ⅲ的名称是 ;操作Ⅱ需要的主要玻璃仪器有 。
⑵加入锌粉的目的是将少量溴化银中的银还原出来,该反应的离子反应方程式为 。
⑶液体B中除含有Br-,还有SO42-,检验溶液中存在SO42-的操作是 。
⑷步骤③实验操作时,也常采用加入适量硝酸钾加盖后再灼热的方法,推测加硝酸钾的目的可能是 。
⑸通过上述回收银的流程中,从绿色化学的要求看,存在的不足为 。
查看答案和解析>>
科目: 来源: 题型:
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3: 2SO2(g)+O2(g)![]() 2SO3(g)。某温度下,SO2的平衡转化率( α)与体系总压强(p)的关系如图所示。根据图示回答下列问题:
2SO3(g)。某温度下,SO2的平衡转化率( α)与体系总压强(p)的关系如图所示。根据图示回答下列问题:
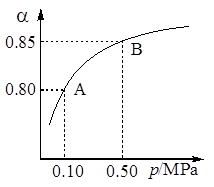
①将2.0 mol SO2和1.0 mol O2置于10 L密闭容器中,反应达平衡后,体系总压强为0.10 MPa。该反应的平衡常数等于____________。
②平衡状态由A变到B时,平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g);DH =-574 kJ/mol
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g);DH =-1160 kJ/mol
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为_____________(阿伏加德罗常数的值用NA表示),放出的热量为_________kJ。
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M = Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。转化流程如图所示:
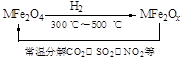
请写出MFe2Ox分解SO2的化学方程式______________________________________(可不配平)。
查看答案和解析>>
科目: 来源: 题型:
已知:(苯胺,易被氧化)。甲苯是一种重要的有机化工原料,可用来合成多种重要的有机物。以甲苯为初始原料合成阿司匹林等有机物的转化关系图(部分产物、合成路线、反应条件略去)如下。
 请回答下列问题:
请回答下列问题:
(1)甲苯的1H核磁共振谱图中有 个特征峰。
(2)中间产物D与目标产物Y的关系是 。
(3)写出结构简式:A ,E 。
(4)写出所加试剂或反应条件:反应⑤ 。
(5)写出反应③的化学方程式:
。
(6)写出阿司匹林与足量的NaOH(aq)反应的化学方程式:
。
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是( )
A.“纳米泡沫”被称为第五形态的单质碳,形似海绵并有磁性,与石墨化学性质完全不同
B.有人建议用液氨作为清洁的汽车燃料,燃烧的最终的产物为氮气和水
C.我国首创用CO2合成可降解的塑料聚二氧化碳,该塑料的结构简式为
D.人造纤维、合成纤维和光导纤维都是有机高分子化合物
查看答案和解析>>
科目: 来源: 题型:
下列判断中一定正确的是( )
A.分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1∶2
B.等质量的O2与O3中,氧原子的个数比为3∶2
C.CaCl2及CaO2固体中阴、阳离子数之比均为2∶1
D.10mL 0.3mol/LNaCl与30mL0.1mol/LAlCl3溶液中Cl-物质的量浓度比为1∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com