
科目: 来源: 题型:
(10分)盐酸、硫酸和硝酸是中学阶段常见的三种强酸。请就三者与金属铜的反应情况,回答下列问题:
(1)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式 。
(2) 若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是 ,反应中所消耗的硝酸的物质的量可能为 .
A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解成蓝色溶液,该反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
19.(12分)某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。
![]()
(1)为完成上述实验,正确的连接顺序为A连_______;B连_______(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为 。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是 ,对应的现象为 。
(4)丙装置的c瓶中盛放的试剂为 ,作用是_______________________。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案
精确测量硬质玻璃管的质量为a g, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g ,实验完毕后
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
①请你分析并回答: 方案测得结果更准确。你认为不合理的方案的不足之处在 。
②按测得结果更准确的方案进行计算,Cu的相对原子质量 。
查看答案和解析>>
科目: 来源: 题型:
(10分)各物质之间的转换关系如下图,部分生成物省略。
已知:①常温下,D、F、G、L为气体;C是日常生活中的常见金属;
②K的应用十分广泛,作为红色颜料跟某些油料混合,可以制成防锈油漆;
③E的水溶液中加盐酸无明显现象,然后加入BaCl2溶液出现浑浊。
请回答下列问题:
(1)写出F的电子式: ;
(2)写出化学式:X 、Y ;
(3)写出C与KOH液反应的化学方程式: ;写出H的稀溶液与I反应的离子方程式: 。
查看答案和解析>>
科目: 来源: 题型:
(9分)烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
⑴烟气脱硫、脱硝的环境意义是 。
⑵选择性催化还原法的脱硝原理为:
6NOx+4xNH3 ![]() (3+2x)N2+6xH2O
(3+2x)N2+6xH2O
①上述反应中每转移3mol电子,生成标准状况下N2的体积为 L。
②已知:2H2(g)+O2(g) =2H2O(g) ΔH=-483.6 kJ·mol-1
N2(g)+3H2(g)=2NH3(g) ΔH=-92.4 kJ·mol-1
N2(g)+O2(g)=2NO(g) ΔH=-180.5kJ·mol-1
则反应6NO(g)+4NH3(g)=5N2(g)+6H2O(g)的ΔH= 。
⑶目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。
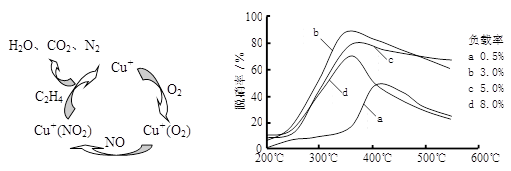
图1 图2
①写出该脱硝原理总反应的化学方程式: 。
②为达到最佳脱硝效果,应采取的条件是 。
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是( )
A.研究物质的性质,常用观察、实验、分类、比较等方法;研究物质的结构,常利用模型、假说等方法
B.丁达尔现象可用于区别溶液与胶体,云、雾均能产生丁达尔现象
C.纤维素、PLA(聚乳酸)、硝化纤维等都是高分子化合物
D.2010年度诺贝尔化学奖者授予三位美日科学家,他们因研究“有机物合成过程中钯催化交叉偶联”,促进了制造复杂化学物质的可能性,化学家们能在试管中制造了非凡的化学“作品”,说明有机反应全部需要催化剂
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是 ( )
A.FeO溶于足量稀HNO3:FeO+2H+=Fe2++H2O
B.NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
C.将0.1mol·L-1的NH4Al(SO4)2溶液与0.2mol·L-1的Ba(OH)2溶液等体积混合:
Al3++2SO42-+2Ba2++4OH-=AlO2-↓+2BaSO4↓+2H2O
D.CuSO4溶液吸收H2S气体 Cu2++H2S=CuS↓+2H+
查看答案和解析>>
科目: 来源: 题型:
麦角醇(ergosterol)在紫外光照射下可转化为抗软骨病的维生素D2,麦角醇的结构为:
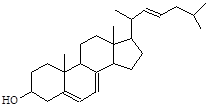
下列关于该化合物的说法不正确的是( )
A.可发生取代、加成、氧化等反应
B.分子式为C27H42O
C.1H核磁共振谱证明分子中的4种不同类型的甲基
D.属于芳香族化合物
查看答案和解析>>
科目: 来源: 题型:
已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3 kJ/mol
③红磷的化学式为P,白磷的化学式为P4,已知
P4(s)+5O2(g)=P4O10(s) △H=-3093.2 kJ/mol
4P (s)+5O2(g)=P4O10(s) △H=-2954.0 kJ/mol
下列结论正确的是( )
A.由于红磷转化为白磷是放热反应,等质量的红磷能量比白磷低
B.稀硫酸与稀NaOH溶液反应的中和热△H=57.3kJ/mol
C.碳的燃烧热大于-110.5 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,△H 大于-57.3 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
下列六个说法可以实现的个数是( )
①酸性氧化物在一定条件下均能与碱发生反应
②弱酸与盐溶液反应可以生成强酸
③发生复分解反应,但产物既没有水生成,也没有沉淀和气体生成
④两种酸溶液充分反应后,所得溶液呈中性
⑤有单质参加的反应,但该反应不是氧化还原反应
⑥两种氧化物发生反应有气体生成
A.6个 B.5个 C.4个 D.不多于3个
查看答案和解析>>
科目: 来源: 题型:
下列实验结论错误的是( )
A.将3~4个火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,若出现白色沉淀,说明含有氯元素
B.制摩尔盐时用酒精洗涤产品
C.制备硫酸亚铁铵晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液表面出现晶膜为止,不能将溶液全部蒸干
D.提取海带中碘元素时,为将I-完全氧化为I2,用HNO3作氧化剂比用H2O2或新制氯水效果好
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com