
科目: 来源: 题型:
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2OCd(OH)2 + 2Ni(OH)2有关该电池的说法正确的 ( )
A.充电时阳极反应:Ni(OH)2-e—+ OH-= NiOOH+H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
查看答案和解析>>
科目: 来源: 题型:
下列溶液中有关微粒的物质的量浓度关系正确的是 ( )
A.常温下物质的量浓度相等的①(NH4)2CO3、②NH4Al(SO4)2、③(NH4)2Fe(SO4)2三种溶液中c (NH4+):③>①>②
B.0.1mol/LNa2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S)
C.常温下将NaHCO3和NaHSO3两溶液混合后,溶液显中性,则混合后的溶液中:c(Na+)=c (HSO3-)+ c (HCO3-)+ 2 c (CO32-)+2 c (SO32-)
D.相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c (H+):①>②>③
查看答案和解析>>
科目: 来源: 题型:
新型解热镇痛抗炎药扑炎痛的结构如图所示,下列关于扑炎痛的叙述正确的是 ( )
A.该物质的分子式为C17H16NO5
B.该物质的核磁共振氢谱上共有9个峰
C.该物质与浓溴水反应生成白色沉淀
D.该物质在酸性条件下水解最终可以得到3种物质
查看答案和解析>>
科目: 来源: 题型:
某密闭容器中加入0.3 mol A、0.1 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[t0~t1阶段 c(B)未画出]。图乙为t2后改变互不相同的某一条件反应速率随时间变化的关系图,t3~t4阶段使用了催化剂。下列说法错误的是( )
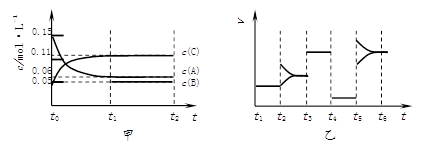
A.若 t1=15 s,生成物C在 t0~t1时间段的平均反应速率为 0.004mol·L-1·s-1
B.t4~t5阶段改变的条件为减小压强,t5~t6改变的条件是升高化学反应的温度
C.B的起始物质的量为0.02mol
D.该化学反应的表达式为:3A B + 2C
查看答案和解析>>
科目: 来源: 题型:
(12分)某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中加入l—2滴溴水,振荡后溶液呈黄色。
(1)提出问题:Fe、Br2谁的氧化性更强?
(2)猜想:
①甲同学认为氧化性:Fe>Br2,故上述实验现象不是发生化学反应所致,则溶液里黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性:Fe<Br2,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
(3)设计实验并验证
丙同学为验证乙同学的观点。选用下列某些试剂设计两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a、酚酞试液 b、四氯化碳 c、无水酒精 d、硫氰化钾溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
|
| 选用试剂 | 实验现象 |
| 方案1 |
|
|
| 方案2 |
|
|
(4)结论氧化性:Fe<Br2,在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为 。
(5)实验后的思考
在2molFeBr2溶液中通入33.6L Cl2(标准状况),所发生的离子反应方程式为 。
查看答案和解析>>
科目: 来源: 题型:
(12分)课外化学兴趣小组欲测定铜锌合金粉末中锌的质量分数。
Ⅰ.除托盘天平必用外,供选择的实验装置如下:
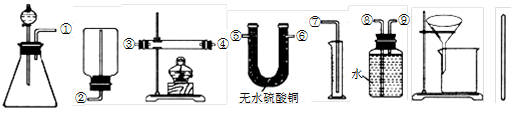
A B C D E F G H
Ⅱ.实验中可测得的数据及其代号如下:
样品的质量m1;充分反应生成的气体体积V(标准状况);反应前仪器和药品的总质量m2;充分反应后仪器和药品的总质量m3;充分反应后剩余固体的质量m4。
(1)实验时必须用到的化学试剂为 。
(2)甲同学实验中使用了A、E、F三种装置,组装时接口编号的连接顺序为: 。样品中锌的质量分数的计算式为 。
(3)乙同学实验中测得的数据为m1和m4,他使用的实验装置有 (填字母)。
(4)丙同学实验中只选用了A装置,他要测得的数据有 (填代号)。
(5)丁同学设计了另一种测定方法,他考虑使用A、C、D三种装置,在C装置中添加足量CuO。除测定m1外,还准备测定C装置反应前后的质量变化。请评价该方法是否可行并说明理由: 。
查看答案和解析>>
科目: 来源: 题型:
10分)下列转化关系图中,A、B、C、D、E常温下为气体,B、E、F、K为单质,其中F为黑色固体;C、D均能使澄清的石灰水变混浊,D、E均能使品红溶液褪色;I是一种红棕色固体氧化物。
请回答下列问题:
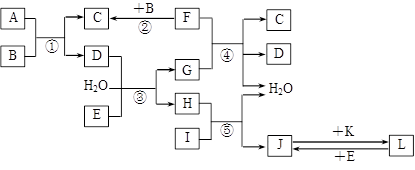
(1)C的电子式为 。
(2)检验溶液L中金属阳离子的方法是 。
(3)反应③的离子方程式为 。
(4)F与G的浓溶液反应的化学方程式为 。
(5)气体A的密度为2.68g·L-1(标准状况),通过计算、推理,可确定A的分子式为 。
查看答案和解析>>
科目: 来源: 题型:
(10分)高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。
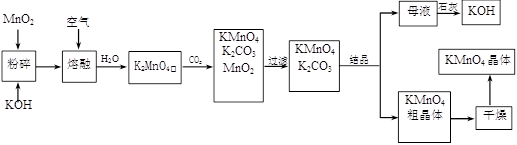
(1)KMnO4稀溶液是一种常用的消毒剂。其消毒机理与下列 (填序号)物质相似。
A.75%酒精 B.双氧水 C.苯酚
D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
。
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是: 。
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、 和 写化学式)。
(5)若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得 mol KMnO4。
查看答案和解析>>
科目: 来源: 题型:
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
(1)烟气脱硫、脱硝的环境意义是 。
(2)选择性催化还原法的脱硝原理为:6NOx+4x NH3 (3+2x)N2+6xH2O
①上述反应中每转移3mol电子,生成标准状况下N2的体积为 L。
②已知:2H2(g)+O2(g) =2H2O (g) ΔH=-483.6 kJ·mol-1
N2(g)+3H2(g)=2NH3(g) ΔH=-92.4kJ·mol-1
N2(g)+O2(g)=2NO(g) ΔH=-180.5kJ·mol-1
则反应6NO(g)+4NH3(g)=5N2(g)+6H2O(g)的ΔH = 。
(3)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。
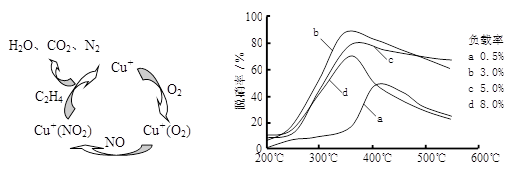
图1 图2
①写出该脱硝原理总反应的化学方程式: 。
②为达到最佳脱硝效果,应采取的条件是 。
查看答案和解析>>
科目: 来源: 题型:
下图为工业制备硝酸的设备示意图,其生产过程中发生的反应主要有:
①4NH3(g)+5O2(g)4NO(g)+6H2O(l) △H<0
②2NO(g)+O2(g)2NO2(g) △H<0
③3NO2(g)+H2O(l)2HNO3(l) +NO(g) △H<0
(1)能使吸收塔内反应速率增大,且能提高HNO3产率的措施是 。
A.适当升高温度 B.适当增大吸收塔内的压强
C.增大空气中O2的浓度 D.吸收塔内填充瓷环,增大气液接触面
(2)在2L密闭容器内充入0.50mol NO和0.25 mol O2,维持反应温度为800℃,当反应达到平衡时,NO的转化率为50%。则800℃时反应2NO+O2=2NO2的平衡常数K= 。
(3)某工厂每套设备每小时可生产20 t 63%的硝酸(密度为1.4 g/cm3)。假设工业生产硝酸过程中,通过循环操作可以使NH3、O2得以完全利用。
回答下列问题:
①该工厂设备所生产硝酸的物质的量浓度是 。
②每小时从吸收塔淋下的水的质量应是多少吨?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com