
科目: 来源: 题型:
钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。V2O5是接触法制硫酸的催化剂。
(1) 一定条件下,SO2 与空气反应t min后,SO2 和SO3 物质的量浓度分别为a mol/L、b mol·L-1,则SO2起始物质的量浓度为_________mol/L ;生成SO3的化学反应速率为_____________________。
(2)全钒液流储能电池是利用不同价态离子对氧化还原反应来实现化学能和电能相互转化的,其装置原理如下图:
① 当左槽溶液逐渐由黄变蓝,其电极反应式为_______________________________。
② 充电过程中,右槽溶液颜色逐渐由__________色变为_______色。
③ 放电过程中氢离子的作用是________________和___________________________;充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为______________。
查看答案和解析>>
科目: 来源: 题型:
2009年4月22日是第40个世界地球日,今年世界地球日的主题是“绿色世纪”。下列行为不符合这一主题的是
A.分类回收、利用垃圾,减少资源浪费
B.推广使用一次性木筷,减少疾病传染
C.开发风能等洁净能源,减少使用化石燃料
D.研究煤和石油脱硫新技术,减少酸雨发生
查看答案和解析>>
科目: 来源: 题型:
设NA表示阿伏加德罗常数的值,下列说法不正确的是
A.1 mol α-氨基乙酸(甘氨酸)分子中存在10 NA对共用电子
B.25℃时,l L pH=13的Ba(OH)2溶液中含有OH-的数目为0.1 NA
C.100mL 3 mol•L-1盐酸与5.6g Fe充分反应转移0.3 NA个电子
D.在标准状况下,22.4L空气中约有NA个气体分子
查看答案和解析>>
科目: 来源: 题型:
用物质的量都是0.1 mol的CH3COOH和CH3COONa配制成1L混合溶液,已知其中C(CH3COO-)>C(Na+),对该混合溶液的下列判断正确的是
A.c(H+)>c (OH-) B. c (CH3COO-)+c(OH-)=0.2 mol/L
C.c (CH3COOH)>c(CH3COO-) D. c (CH3COOH)+c (CH3COO-)=0.2 mol/L
查看答案和解析>>
科目: 来源: 题型:
市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li![]() 的高分子材料。这种锂离子电池的电池反应为:Li+2Li
的高分子材料。这种锂离子电池的电池反应为:Li+2Li![]() 。下列说法不正确的是
。下列说法不正确的是
A.放电时,负极的电极反应式:Li-e![]() =Li
=Li![]()
B.该电池不能用水溶液作为电解质
C.放电过程中Li![]() 向负极移动
向负极移动
D.充电时,Li![]() 既发生氧化反应又发生还原反应
既发生氧化反应又发生还原反应
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分。X、Y、Z、W均为短周期元素,X、W的质子数之和为23。下列说法正确的是
|
| X |
| Y |
| Z |
| W |
|
A.X元素最多可形成五种氧化物
B.W元素的非金属性比Z元素非金属性弱
C.Z和X能以共价键结合形成一种无机非金属材料
D.Y元素的最高价氧化物的水化物是含氧酸中酸性最强的
查看答案和解析>>
科目: 来源: 题型:
下列离子组在指定溶液中能大量共存的是
A.常温时,在c(H+)=![]() 的溶液:Na+、Fe3+、NO3-、Cl-
的溶液:Na+、Fe3+、NO3-、Cl-
B.含大量Fe2+的溶液:Na+、Mg2+、H+、NO3-
C.含有大量Al3+的溶液:K+、Na+、AlO2-、SO42-
D.在c(H+)/c(OH-) = 1×1013的溶液:NH4+、Mg2+、C1-、K+
查看答案和解析>>
科目: 来源: 题型:
在200 mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。
下列叙述正确的是
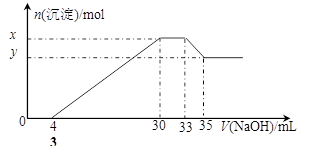
A.原溶液的pH=2
B.原溶液中c(Cl-)=0.75 mol·L-1
C.x与y的差值为0.01 mol
D.原溶液中n(Mg2+)∶n(Al3+)=5∶2
查看答案和解析>>
科目: 来源: 题型:
温度为t℃,压强为1.01×106Pa的条件下,某密闭容器内,下列反应达到化学平衡:A(g) + B(g) 3C,测得此时c(A)=0.022mol·L-1;压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得c(A)=0.05mol·L-1;若继续压缩容器,使压强增大到4.04×107Pa,第三次达到平衡时,测得c(A)=0.75mol·L-1;则下列关于C物质状态的推测正确的是
A.每次平衡时C均为非气态 B.每次平衡时C均为气态
C.第二次达到平衡时C为非气态 D.第三次达到平衡时C为非气态
查看答案和解析>>
科目: 来源: 题型:
(18分)
张明同学对硫酸及其盐的某些性质中进行了如下实验探究。
[实验一]探究浓硫酸的氧化性
将实验室常用的药品放入如右图所示的实验装置后,加热装置甲。(夹持和加热装置省略)
(1)该装置设计上存在明显缺陷,其缺陷是 _________________________________ ___。
(2)装置甲中反应的化学方程式是___________ ___。
(3)装置乙中的试剂是_____________________________________________________。
[实验二]探究某硫酸亚铁盐固体是否变质
(4)请你帮助张明同学完成如下实验方案:
| 实验操作 | 预期现象和结论 |
|
|
|
[实验三]用KHSO4制取H2O2并测其质量分数
查阅资料得知:工业上用电解KHSO4饱和溶液制取H2O2,示意图如下:
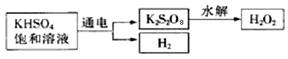
张明用此法制取一定浓度的H2O2,并进行下列实验测定H2O2的质量分数:(离子方程式:2MnO4―+5H2O2+6H+=2Mn2++8H2O+5O2↑)
①取5.00 mL H2O2溶液(密度为1.00 g/mL)置于锥形瓶中加水稀释,再加稀硫酸酸化;
②用0.1000 mol/L KMnO4溶液滴定;
③用同样方法滴定,三次消耗KMnO4溶液的体积分别为20.00mL、19.98 mL、20.02 mL。
请回答:
(5)电解饱和KHSO4溶液时,阳极的电极反应式为____________________________。
(6)操作②中,滴入第一滴KMnO4溶液,溶液紫红色消失很慢,随着滴定过程中Mn2+的增多,溶液紫红色消失速率加快。Mn2+的作用是_____________ ___。
(7)原H2O2溶液中溶质的质量分数是__________ _____ ____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com