
科目: 来源: 题型:
把80mlNaOH溶液加入到120ml盐酸中,所得溶液的PH值为2(设混合后溶液总体积为原溶液体积之和)。如果混合前NaOH溶液和盐酸的物质的量浓度相同,它们的浓度是( )
A.0.05mol/L B.0.1mol/L C.1.0mol/L D.0.5mol/L
查看答案和解析>>
科目: 来源: 题型:
mA(s)+nB(g) pC(g);ΔH<0,在室温条件下B的体积分数(B%)与压强(P)的关系如图所示。
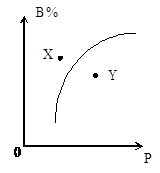
则下列有关叙述中一定正确的是( )
①m+n<p ②X点时的正反应速率大于逆反应速率
③X点比Y点时的反应速率慢 ④若升高温度,该反应的平衡常数增大
A.①②③ B.②③④ C.只有②③ D.①②④
查看答案和解析>>
科目: 来源: 题型:
下列各溶液中,微粒的物质的量浓度关系正确的是( )
A. 0.1 mol /L的(NH4)2SO4溶液中:c (SO42—)> c(NH4+ )> c (H+)> c (OH—)
B. 0.2 mol /L的Na2CO3溶液中:c (OH—)= c (HCO3—)+c (H+)+ c (H2CO3)
C. 0.1 mol /L的NH4Cl溶液与0.05 mol L-l的NaOH溶液等体积混合,其混合溶液中:
c (Cl-) > c (NH4+) > c (Na+ ) > c (H+) > c(OH-)
D. c (NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4C1溶液中:
c [(NH4)2SO4]< c [(NH4)2CO3] < c (NH4C1)
查看答案和解析>>
科目: 来源: 题型:
广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述观点下列说法不正确的是( )
A. PCl3的水解产物是PH3和HClO B.NaClO的水解产物之一是HClO
C. CaO2的水解产物是Ca(OH)2和H2O2 D.Mg3N2水解生成NH3和Mg(OH)2
查看答案和解析>>
科目: 来源: 题型:
将0.2mol·L-1HCN溶液和0.1mol·L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是( )
A.c(HCN)<c(CN-) B.c(Na+)<c(CN-)
C.c(HCN)-c(CN-)=c(OH-) D.c(HCN)+c(CN-)=0.1mol·L-1
查看答案和解析>>
科目: 来源: 题型:
在一固定体积的密闭容器中加入2 mol A和1 mol B发生反应2A(g)+B(g) 4C(g)+D(s),达到平衡时C的浓度为w mol·L-1,若维持容器的体积和温度不变,按下列四种配比方案作为反应物,达平衡后,使C的浓度仍为wmol·L-1的配比是( )
A.4 molA+2 molB B.4 mol C+1 molD+2mol A+1 mol B
C.4 molC+1.5 molD D. 4 mol C+0.8mol D
查看答案和解析>>
科目: 来源: 题型:
(10分)(1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
①丙烷脱氢可得丙烯。已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6kJ·mol-1
CH3CH=CH2(g)→CH4(g)+HC≡CH(g) △H2=+32.4kJ·mol-1
则相同条件下,反应C3H8(g)→CH3CH=CH2 (g)+H2(g)的△H= kJ·mol-1。
②以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应总方程式为
;放电时CO32-移向电池的 (填“正”或“负”)极。
(2)反应A(g)+B(g)C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

①该反应是_______________反应(填“吸热”“放热” );
②在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”“减小”“不变” );
③反应体系中加入催化剂对反应热是否有影响?_____________,原因是______________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(6分)在一个密闭容器中,保持一定的温度和压强进行以下反应:
A(g) +3B(g) 3C(g),已知加入1 molA和3 molB,平衡时A的物质的量为a mol。
(1)达到平衡时C在反应混合体中体积百分含量是 (用含a的关系式表示)
(2)在相同的实验条件下,若在同一个容器中改为加入2 molA和6molB,达到平衡后, C在混合气体中的体积百分含量 (填“增大”“减小”或“不变”)。
(3)在相同的实验条件下,如果加入n mol A、mmol B和p molC,若要求平衡后C在混合气体中的百分含量保持不变,与(1)相同,则n、m与p的关系式为 。
查看答案和解析>>
科目: 来源: 题型:
(9分)将等物质的量的A、B、C、D四种物质混和,发生如下反应: aA+bBcC(固)+dD当反应进行一定时间后,测得A减少了nmol,B减少了n/2 mol,C增加了3n/2 mol,D增加了nmol,此时达到化学平衡:
(1)该化学方程式中各物质的系数为a=_______,b=______,c_______,d=__ ___。
(2)若只改变压强,反应速率发生变化,但平衡不发生移动,该反应中各物质的聚集状态A_______,B________,D_________。
(3)该反应的平衡常数表达式为K= 。若升高温度,达到平衡后平衡常数减小,则该反应为________反应(填放热或吸热)
查看答案和解析>>
科目: 来源: 题型:
(8分)已知由短周期元素组成的A、B、C、D四种常见化合物分子中所含原子数目依次为2、3、4、5,其中A、B含有18个电子,C、D含有10个电子。请回答:
(1)D中含有的化学键类型有 ,已知8gD与O2完全燃烧,生成稳定化合物时放出445kJ的热量,写出反应的热化学方程式 。
(2)室温下,若向一定量C的稀溶液中逐滴加入物质的量浓度相同的A,直至A过量,生成化合物XY4Z(X、Y、Z表示元素符号)。讨论上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH。试填写表中空白(要求填写有关粒子化学式):
|
| 离子浓度由大到小的顺序 | 溶质的化学式 | 溶液的pH |
| I | c(XY+4)>c(Z—)>c(OH—)>c(H+) |
| pH>7 |
| II | c(XY+4)=c(Z—) | XY4Z、XY3·H2O |
|
| III |
| XY4Z | pH<7 |
| IV | c(Z—)>c(H+)>c(XY+4)> >c(OH—) |
| pH<7 |
(3)B在空气中完全燃烧生成E,在一定条件下发生E与O2反应生成F。
①将0.05molE和0.03molO2放入容积为1L的密闭容器中,达到平衡,测得c(F)=0.04mol·L—1。计算该条件下反应的平衡常数K= 和E的平衡转化率 。
②已知上述反应是放热反应,当该反应处于平衡状态时,下列措施中有利于提高E平衡转化率的有 (填字母)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com