
科目: 来源: 题型:
已知:H2(g)+Cl2(g)==== 2HCl(g) ΔH=-183 kJ/mol ,下列说法正确的是( )
A.2L氯化氢气体分解成1L的氢气和1L的氯气,吸收183kJ热量
B.1mol氢气与1mol氯气反应生成2mol液态氯化氢放出的热量小于183kJ
C.在相同条件下,1mol氢气与1mol氯气的能量总和大于2mol氯化氢气体的能量
D.1个氢气分子与1个氯气分子反应生成2个氯化氢分子放出183kJ热量
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式中的反应热下划线处表示燃烧热的是( )
A.C6H12O6(s)+6O2(g)6CO2(g)+6H2O(g);ΔH=-akJ·mol-1
B.CH3CH2OH(l)+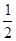 O2(g)
O2(g)CH3CHO(l)+H2O(l);ΔH=-bkJ·mol-1
C.CO(g)+ ![]() O2(g)
O2(g) CO2(g);ΔH=-c kJ·mol-1
D. 2H2(g)+O2(g)=2H2O(l);ΔH=-d kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
已知:(1)Zn(s)+1/2O2(g) = ZnO(s) △H =-348.3 kJ/mol
(2) 2Ag(s)+1/2O2(g) = Ag2O(s) △H =-31.0 kJ/mol
则Zn(s)+Ag2O(s) =ZnO(s)+2Ag(s)的△H等于( )
A. -317.3kJ/mol B. -379.3kJ/mol
C. -332.8kJ/mol D. 317.3 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
将4 molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)2C(g)。若经2s(秒)后测得 C 的浓度为0.6mol·L-1 ,现有下列几种说法,其中正确的是( )
①用物质A表示该反应的平均速率为0.3mol·L-1·s-1;
②用物质B表示的反应的平均速率为0.6mol·L-1·s-1;
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol·L-1;
A.①③ B.①④ C. ②③ D. ③④
查看答案和解析>>
科目: 来源: 题型:
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8kJ/mol、890.3 kJ/mol、2800kJ/mol,则下列热化学方程式正确的是( )
A.C(s)+1/2 O2(g)=CO(g) △H= ―393.5 kJ/mol
B.2H2(g)+O2(g)=2H2O(l) △H= +571.6 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= ―890.3 kJ/mol
D.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) △H= ―2800 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是( )
A.需加热才能发生的反应一定是吸热反应
B.任何放热反应在常温条件一定能发生反应
C.反应物和生成物分别具有的总能量决定了反应是放热反应还是吸热反应
D.ΔH的大小与热化学方程式的计量系数无关
查看答案和解析>>
科目: 来源: 题型:
已知(1)H2O(g) == H2O(l) ΔH1=-Q1 kJ·mol-1
(2)CH3OH(g) == CH3OH(l) △H2=-Q2kJ·mol-1
(3)2CH3OH(g) +3O2(g) == 2CO2(g)+4H2O(g) △H3=-Q3kJ·mol-1
(Q1、Q2、Q3均大于0)若要使32g液态甲醇完全燃烧,最后恢复到室温,放出的热量为(单位:kJ) ( )
A. Q1+Q2+Q3 B. 0.5 Q3-Q2+2Q1 C. 0.5 Q3+ Q2-2Q1 D. 0.5(Q1+Q2+Q3)
查看答案和解析>>
科目: 来源: 题型:
下列说法或表示法正确的是
A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨)→C(金刚石) ΔH = +119kJ·mol—1可知,金刚石比石墨稳定
C.在稀溶液中:H++OH-===H2O ΔH = -57.3 kJ· mol—1,若将含1mol CH3COOH的醋酸溶液与含1mol NaOH的溶液混合,放出的热量小于57.3 kJ
D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+ O2(g)==2H2O(l) ΔH = +285.8 kJ· mol—1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com