
科目: 来源: 题型:
下列事实不能用勒夏特列原理解释的是( )
A.由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
B.黄绿色的氯水光照后颜色变浅
C.使用催化剂可加快SO2转化为SO3的速率
D.在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目: 来源: 题型:
密闭容器中一定量的混合气体发生反应:xA(g)+yB(g) zC(g),平衡时,测得A的浓度为0.80mol·L-1,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,A的浓度为0.30mol·L-1,有关叙述正确的是( )
A.平衡向逆反应方向移动 B.x + y < z
C.B的转化率降低 D.C的体积分数增大
查看答案和解析>>
科目: 来源: 题型:
下列有关叙述中正确的是( )
A、难溶于水的电解质一定是弱电解质
B、强电解质的水溶液导电能力不一定比弱电解质水溶液的导电能力强
C、易溶于水的电解质一定是强电解质
D、强电解质在水溶液中的电离过程是不可逆的
查看答案和解析>>
科目: 来源: 题型:
25 ℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应生成1mol水时所放出的热量约为57.3 kJ/mol;辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是( )
A.CH3COOH(aq)+NaOH(aq)===CH3COONa(aq)+H2O(l) ![]() H=
H=![]() 57.3kJ/mol
57.3kJ/mol
B.KOH(aq)+![]() H2SO4(aq)=
H2SO4(aq)=  K2SO4(aq)+H2O(l)
K2SO4(aq)+H2O(l) ![]() H=
H=![]() 57.3kJ/mol
57.3kJ/mol
C.2C8H18(g)+25O2(g)=16CO2 (g)+18H2O(1) 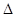 H=
H=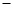 11036kJ/mol
11036kJ/mol
D.C8H18(l)+ ![]() O2 (g)=8CO2 (g)+9H2O(g)
O2 (g)=8CO2 (g)+9H2O(g) 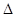 H=
H=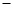 5518 kJ/mol
5518 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
⑴(3分)常温、101kPa,15g乙烷完全燃烧放出的热量为390.2 kJ,则乙烷完全燃烧的热化学方程式为:
⑵(4分)把煤作为燃料可通过下列两种途径:途径Ⅰ:C(s)+O2(g)=CO2(g) ΔH1<0 ①途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) ΔH2>0 ②
再燃烧水煤气:CO(g)+  O2(g)=CO2(g) ΔH3<0 ③
O2(g)=CO2(g) ΔH3<0 ③
H2(g)+ ![]() O2(g)=H2O(g) ΔH4<0 ④
O2(g)=H2O(g) ΔH4<0 ④
请回答下列问题:
①途径Ⅰ放出的热量__________(填“大于”、“等于”或“小于”)途径Ⅱ放出的热量。
②用ΔH2、ΔH3、ΔH4表示ΔH1的数学关系式是_______________
查看答案和解析>>
科目: 来源: 题型:
一密封体系中发生反应:N2 +3H2 ![]() 2NH3 ΔH<0,
2NH3 ΔH<0,
①以下图1、图2均表示该反应在t1时达到平衡,在t2时改变某条件发生变化的曲线。

试判断,图1中t2时改变的条件是______________ ;图2中t2时改变的条件是____ _________。
②下图是某一时间段中反应速率与反应进程的曲线关系图:
下列各时间段时,氨的百分含量最高的是 。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
③工业生产中提高合成氨反应的反应速率和产率的具体措施是:
A.降低温度 B. 增大压强 C. 降低压强
D. 循环利用和不断补充氮气 E. 及时移出氨气
查看答案和解析>>
科目: 来源: 题型:
⑴(7分)高温下,某反应达到平衡,平衡常数K=。
①该反应化学方程式为 。
②若恒容时,温度升高,H2浓度减小,则该反应焓变为 (填正值或负值)。
③恒温恒压下,若继续向原平衡混合物的容器中通入少量氦气(假设氦气和各物质不反应)后,化学平衡 移动;反应物的转化率 (填增大、减小、或不变);H2的浓度
(填增大、减小、或不变);
⑵(6分)可逆反应: X+ 3Y(g) 2Z(g) +2W(g)达到平衡,混
合物中Y的体积分数随压强(P)与温度T(T2>T1)的变化关系如图示。
①当压强不变时,升高温度,Y的体积分数变 ,
平衡向 方向移动,则正反应是 热反应。
②当温度不变时,增大压强,Y的体积分数变 ,
平衡向 方向移动,则X的状态是
查看答案和解析>>
科目: 来源: 题型:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
⑴从实验装置上看,图中尚缺少的一种玻璃用品是 。
⑵烧杯间填满碎纸条的作用是 。
⑶如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由 。
⑷用相同浓度和体积的醋酸溶液代替盐酸进行上述实验,测得的中和热ΔH会 。(填“偏大”、“偏小”、“无影响”)
查看答案和解析>>
科目: 来源: 题型:
某化学反应2AB+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内A的平均速率为_________mol/(L·min)。
(2)在实验2,A的初始浓度c2=_________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_________。
(3)设实验3的反应速率为υ3,实验1的反应速率为υ1,则υ3_________υ1(填>、=、<),且c3_________1.0 mol/L(填>、=、<)。
(4)比较实验4和实验1,可推测该反应是_________反应(选填吸热、放热)。理由是:
______________________________________________________________________
查看答案和解析>>
科目: 来源: 题型:
t℃时,将3mol A和1mol B气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g) xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1,请填写下列空白,并利用三段式写出①②的计算过程。
①从开始反应至达到平衡状态,求反应物A的平均反应速率和A的转化率。
②求x的值和t℃该反应的平衡常数K的值。
③若向原平衡混合物的容器中再充入4 mol C,在t℃时达到新的平衡,此时B的物质的量为n(B)= mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com