
科目: 来源: 题型:
室温下,某溶液中由水电离出来的c(H+)为1×10-12 mol/L,则该溶液中一定不可能大量存在的离子组是
A.Cu2+、SO42-、Cl-、Na+ B.Ca2+、Cl-、HCO3-、K+
C.NH4+、NO3-、SO42-、Mg2+ D.Cl-、SO42-、K+、Na+
查看答案和解析>>
科目: 来源: 题型:
对于相同物质的量浓度、相同体积的盐酸和醋酸,下列几种说法正确的是
A.它们起始时溶液中的c(H+)相同
B.各用水稀释一倍后,pH比较:盐酸>醋酸
C.分别和同浓度的氢氧化钠溶液反应至pH=7,所用氢氧化钠溶液的体积不同
D.各与足量的锌粒充分反应,产生H2的量不同
查看答案和解析>>
科目: 来源: 题型:
常温下,0.1 mol/L某一元酸(HA)溶液中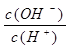 =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
A.HA为强酸
B.溶液中c(H+)+c(A—)=0.1 mol/L
C.溶液中加入一定量CH3COONa晶体,溶液的c(OH—)增大
D.与0.05mol/LNaOH溶液等体积混合后所得溶液中离子浓度大小关系为
c(A—)>c(Na+)>c(OH—)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是
A.生成了一种强酸弱碱盐
B.弱酸溶液和强碱溶液反应
C.一元强酸溶液和强碱溶液反应
D.二元强酸溶液和强碱溶液反应
查看答案和解析>>
科目: 来源: 题型:
用已知浓度的酸滴定未知浓度的碱时,会导致待测碱液浓度偏低的操作是
A.碱式滴定管用蒸馏水洗后,未用待测液润洗
B.酸式滴定管用蒸馏水洗后,未用标准液润洗
C.滴定前,锥形瓶用蒸馏水洗后未烘干
D.滴定前酸式滴定管尖嘴部分未充满溶液
查看答案和解析>>
科目: 来源: 题型:
如图,图Ⅰ表示10 mL量筒中液面的位置,A与B、B与C刻度间相差1 mL,图II表示50mL滴定管中液面的位置,D与E刻度间相差1 mL。如果刻度A和D都是4,则两处液面的读数是
A.Ⅰ中是3.2 mL,Ⅱ中是5.40 mL
B.Ⅰ中是4.8 mL,Ⅱ中是3.40 mL
C.Ⅰ中是3.2 mL,Ⅱ中是4.60 mL
D.Ⅰ中是4.8 mL,Ⅱ中是4.60 mL
查看答案和解析>>
科目: 来源: 题型:
(填化学式)在空气中:将氯化铁溶液蒸干并灼烧得到的固体物质_______________;碳酸氢钠溶液蒸干并灼烧得到的固体物质_____________;硫酸铝溶液蒸干得到的固体物质___________________;亚硫酸钠溶液蒸干得到的固体物质 __________ 。
查看答案和解析>>
科目: 来源: 题型:
水的电离平衡曲线如下图所示。?
(1)若以A点表示25℃时水在电离平衡时的离子浓度, 当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 。
(2)将常温下的pH=8的Ba(OH)2溶液与常温下的pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为 。
查看答案和解析>>
科目: 来源: 题型:
恒温、恒压下,在一个可变容积的容器中发生如下发应:
2 A(g)+ B(g) 2 C(g)
(1)若开始时放入2 mol A和1 mol B,到达平衡后,生成a mol C,这时A的物质的
量为 mol。
(2)若开始时放入6 mol A和3 mol B,到达平衡后,生成C的物质的量为 mol。
(3)若开始时放入x mol A,2 mol B和2 mol C,到达平衡后,A和C的物质的量分别是y mol和3 a mol,则x= mol。
(4)若在(3)的平衡混合物中再加入1 mol C,待再次到达平衡后,C的物质的量分数是 。
查看答案和解析>>
科目: 来源: 题型:
NaHCO3在水溶液中,HCO3-的电离程度小于HCO3-的水解程度。回答下列有关问题:
⑴H2CO3的电离方程式为 ;
⑵NaHCO3溶液显碱性,原因是(用离子方程式表示)
;
⑶在该溶液中,c(Na+)、c(H+)、c(HCO3-)、c(OH-)的大小关系为
;
⑷根据电荷守恒原理,该溶液中离子浓度关系有:
c(Na+)+c(H+)= ;
⑸根据物料守恒原理,该溶液中离子浓度关系有:
c(Na+)= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com