
科目: 来源: 题型:
化学与社会、生活密切相关,下列有关说法不正确的是 ( )
A.利用清洁能源代替化石燃料,有利于节约资源、保护环境
B.食品添加剂种类很多,其中的一种为苯甲酸钠,它是苯的一种同系物所对应的钠盐
C.抗酸药的种类很多,如碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝、氢氧化镁等
D.乙醇属于可再生能源
查看答案和解析>>
科目: 来源: 题型:
下列有关物质分类或归纳的说法中,正确的一组是 ( )
①蔗糖和麦芽糖的化学式都可用C12H22O11表示,它们互为同分异构体
②聚乙烯、聚氯乙烯、纤维素都属于合成高分子
③明矾、石膏、冰醋酸、水都是电解质
④盐酸、漂白粉、水玻璃都是混合物
⑤分馏、干馏、裂化都是化学变化
⑥植物油、直馏汽油都可与溴水反应
A.①③⑤ B.②④⑥ C.①③④ D.②⑤⑥
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述中正确的是 ( )
①12.4g白磷晶体中含有的P-P键数约是0.6 NA
②电解精炼铜时转移了NA个电子,阳极溶解32 g铜
③7.8 g Na2S和Na2O2的固体混合物中含有的阴离子数大于0.1 NA
④CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)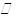 2CO(g)+O2(g) △H=+2×283.0kJ/mol
2CO(g)+O2(g) △H=+2×283.0kJ/mol
⑤2.9g 2CaSO4·H2O含有的结晶水分子数为0.02 NA
⑥含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
⑦含0.1mol溶质Na2CO3的溶液中,所含阴离子总数大于0.1NA
A.①④⑤⑦ B.①④⑦ C.①③④⑤⑥ D.②③⑤⑥
查看答案和解析>>
科目: 来源: 题型:
下列各组离子在指定溶液中,能大量共存的是 ( )
A.强碱性溶液中:K+,ClO-,Ba2+,Cl-
B.水电离的H+浓度c(H+)=10-12mol·L-1的溶液中:Cl-,CO32-,NO3-,NH4+
C.使甲基橙变红的溶液中:Fe2+,MnO4-,NO3-,Na+
D.中性溶液中:Al3+,NO3-,Cl-,S2-
查看答案和解析>>
科目: 来源: 题型:
海南的毒豇豆、毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如图所示:对该化合物的叙述正确的是 ( )
A.该化合物属于芳香烃
B.该化合物的分子式为C11H14O4NPS
C.该化合物能发生加聚反应、水解反应和酯化反应
D.该化合物中至少有7个碳原子在同一平面
查看答案和解析>>
科目: 来源: 题型:
下列图象能表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)( )
A.图1:n(HCl)=1mol,K2CO3加入到HCl溶液中,在敞口容器中生成的气体
B.图2:n(NaOH)=1mol,CO2通入到NaOH溶液中反应生成的盐
C.图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物
D.图4:n(HNO3)=1mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO)
查看答案和解析>>
科目: 来源: 题型:
常温下,向一定浓度的醋酸溶液中逐滴加入氢氧化钠溶液直至过量,在此操作过程中,有关溶液中离子浓度变化的大小关系不正确的是 ( )
A.当pH=7时,c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
B.当pH>7时,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.当恰好完全中和时,c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.反应全程都有关系:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
查看答案和解析>>
科目: 来源: 题型:
(14分)
甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,来制备甲醇。
(1)将1.0 mol CH4和2.0 mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应:CH4(g)+H2O(g) CO(g)+3H2(g)……Ⅰ,CH4的转化率与温度、压强的关系如右图所示:
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为 。
②图中的P1 P2(填“<”、“>”或“=”),100℃时平衡常数为 。
(2)在压强为0.1 MPa条件下, a mol CO与 3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g) CH3OH(g) ……Ⅱ。
③该反应的△H 0,△S 0(填“<”、“>”或“=”)。
④若容器容积不变,下列措施可增加甲醇产率的是
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
(3)在最新开发并投入生产的流动电解质直接甲醇燃料电池中,流动电解质硫酸的使用,可提高燃料电池效率约30%,该电池的负极反应为 。
查看答案和解析>>
科目: 来源: 题型:
(14分)
A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,其中B、D属于常见金属,其余均为常见化合物,J是一种黑色固体,I的浓溶液具有还原性,A—J的所有物质之间有如下的转化关系(部分反应产物省略):
(1)B元素和C元素的简单离子半径大小关系是(用离子符号表示): _;
(2)将氮元素与C形成的化合物NC3加入水中产生使红色石蕊试纸变蓝的气体,写出该反应的化学方程式 ;
(3)由E的饱和溶液滴入沸水中形成透明液体,再将此液体装入U型管,并在U型管的两端插入电极,接通直流电,在阳极端可观察到的现象是______________ ___;
(4)将适量J加入酸化的H2O2的溶液中,J溶解生成它的+2价离子,该反应的离子方程式是__________________________________________________ _;
(5)向含有0.1 mol G的溶液中滴加5 mol/L 的盐酸溶液,得到沉淀3.9 g ,则加入盐酸的体积可能为______________________________(mL)。
查看答案和解析>>
科目: 来源: 题型:
(15分)
为了证明化学反应有一定的限度,进行了如下探究活动:
(Ⅰ)取5mL0.1mol·L-1的KI溶液,滴加0.1 mol·L-1的FeCl3溶液5~6滴
(Ⅱ)继续加入2mLCCl4振荡
(Ⅲ)取萃取后的上层清液,滴加KSCN溶液
(1)探究活动(Ⅰ)和(Ⅱ)的实验现象分别为_____________、 。
(2)在探究活动(Ⅲ)中,活动设计者的意图是通过生成血红色的Fe(SCN)3,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中,却未见溶液呈血红色,对此同学们提出了下列两种猜想。
猜想一:Fe3+已全部转化为Fe2+
猜想二:生成Fe(SCN)3浓度极小,其颜色肉眼无法观察
为了验证猜想,在查阅资料后,获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高
结合新信息,请你设计以下实验验证猜想
①请将相关的实验操作、现象和结论填入下表
| 实验操作 | 现象 | 结论 |
| 步骤一: | 产生蓝色沉淀 |
|
| 步骤二: |
| “猜想二”成立 |
②写出操作“步骤一”中发生反应的离子方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com