
科目: 来源: 题型:
下面关于SiO2晶体网状结构的叙述正确的是
A.存在四面体结构单元,O处于中心,Si处于4个顶角
B.最小的环上,有3个Si原子和3个O原子
C.最小的环上,Si和O原子数之比为1:2
D.最小的环上,有6个Si原子和6个O原子
查看答案和解析>>
科目: 来源: 题型:
(10分)现有下列几种常见的物质:①N2 ②NaCl ③Ca(OH)2 ④金刚石⑤SiC ⑥NH3 ⑦NH4Cl ⑧CO2。其中,(以下空格均填写序号)
(1)含有非极性键的分子晶体是 ;
(2)含有极性键的分子晶体是 ;
(3)只含离子键的离子晶体是 ;
(4)含有极性共价键的原子晶体是 ;
(5)既含有离子键,又含有极性共价键和配位键的离子晶体是
查看答案和解析>>
科目: 来源: 题型:
(10分)第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图。
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na——Ar之间六种元素用短线连接起来,构成完整的图像。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是
。
(3)上图中6号元素在周期表中的位置是 ;
其原子M层电子的轨道表示式为 。
(4)上图中4,5,6三种元素的气态氢化物的沸点均比同主族上一周期的元素气态氢化物低很多,原因是: 。
查看答案和解析>>
科目: 来源: 题型:
(10分)A、B、C、D、E、F都是短周期元素,原子序数依次增大,B、C、D同周期,A、E同主族。A、C能形成两种液态化合物甲和乙,原子个数比分别为2∶1和1∶1。B元素原子有两个未成对电子,D是周期表中电负性最大的元素,F是地壳中含量最多的金属元素。根据以上信息回答下列问题:
⑴ 比较C、D对应氢化物的稳定性 (填分子式)
⑵ 甲、乙两分子中含有非极性共价键的是 (填分子式),它的电子式为 。
⑶ C、D、E、F的离子中,半径最小的是 (填离子符号)
(4)B的氢化物的空间构型是
查看答案和解析>>
科目: 来源: 题型:
(10分) Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
① Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布msnmpn;
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)Z2+ 的核外电子排布式是 。
(2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。(填写序号)
a.稳定性:甲>乙,沸点:甲<乙 b.稳定性:甲>乙,沸点:甲>乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(3)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为 。
(4)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于 ;1 mol该晶体中含有 mol的化学键
查看答案和解析>>
科目: 来源: 题型:
(10分)中国古代四大发明之一——黑火药,它的爆炸反应为
①除S外,上列元素的电负性从大到小依次为 。
②在生成物中,A的晶体类型为 A的电子式为
③。原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为 ,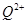 的未成对电子数是 。
的未成对电子数是 。
查看答案和解析>>
科目: 来源: 题型:
氮气是一种很不活泼的气体,其根本原因是
A.氮元素的非金属性较弱 B.氮原子半径小,核对外层电子吸引力较强
C.氮气为双原子分子 D.使N≡N键断裂需要很高的能量
查看答案和解析>>
科目: 来源: 题型:
高空大气中 O2的吸收紫外线后可变成臭氧O3,O3可分解:O3→ O2 + O,O3又和大气污染物如超音速飞机排放的NO发生反应:NO +O3→NO2 + O2,NO2 + O→ NO + O2 ,从反应的全过程判断NO的作用是
A.中间产物 B.氧化剂 C.最终产物 D.催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com