
科目: 来源: 题型:
下列对化学平衡移动的分析中,不正确的是
①已达平衡的反应C(s)+H2O(g)CO(g)+H2(g),当增加反应物的物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g)2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
A.①④ B.①②③ C.②③④ D.①②③④
查看答案和解析>>
科目: 来源: 题型:
用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是
A.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.未用标准液润洗碱式滴定管
查看答案和解析>>
科目: 来源: 题型:
在一定条件下,将1 mol CO和1 mol水蒸气通入容器中发生下述反应:CO+H2OCO2+H2,达到平衡后,测得CO2 0.6 mol;再通入0.3mol水蒸气,又达到平衡后,CO2的物质的量为
A.0.7mol B.0.8mol C.0.6mol D.0.9mol
查看答案和解析>>
科目: 来源: 题型:
(8分)下列物质中:(填序号)
A.KCl(s) B.C2H5OH(l) C. Cl2(g) D.冰醋酸 E.BaSO4(s)
F.NaHSO4(s) G.石墨(s) H.蔗糖(s) I.NaOH溶液
(1)能直接导电的是 ; (2)属于强电解质的是 ;
(3)属于弱电解质的是 ; (4)属于非电解质的是 。
查看答案和解析>>
科目: 来源: 题型:
(10分)写出下列物质的电离方程式(在水溶液中)。
(1)H2SO4 ;
(2)H2CO3 ;
(3)NaHSO4 ;
(4)NaHCO3 ;
(5)Cu(OH)2 。
查看答案和解析>>
科目: 来源: 题型:
(4分)已知下列反应的反应热:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H=-870.3kJ∕mol
②C(S)+O2(g)=CO2(g) △H=-393.5kJ∕mol
③2C(S)+2H2(g)+O2(g)=CH3COOH(l) △H=-488.3kJ∕mol
请写出H2燃烧热的热化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
(12分)在800℃时,2L密闭容器内,2NO(g)+O2(g)2NO2(g)反应体系中,n(NO)随时间的变化如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= 。
已知:![]() >
>![]() ,则该反应是 热反应。
,则该反应是 热反应。
(2)上图中表示NO2的变化的曲线是 ;
用O2表示从0~2 s内该反应的平均速率v= 。
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目: 来源: 题型:
(8分)水的电离平衡曲线如图所示。
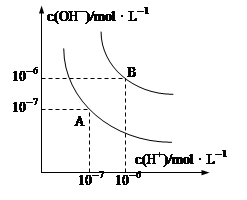
(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 。
(2)将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=7,则Ba(OH)2溶液与盐酸的体积比为 。
(3)已知AnBm的离子积=[c(Am+)]n·[c(Bn-)]m,式中c(Am+)n和c(Bn-)m表示离子的物质的量浓度。在某温度下,Ca(OH)2的溶解度为0.74g,其饱和溶液密度设为1g/mL,其离子积为 。(原子量Ca:40,O:16,H:1)
查看答案和解析>>
科目: 来源: 题型:
N2和H2发生合成氨反应N2(g)+3H2(g)2NH3(g)。在一定条件下达到平衡时,各物质的浓度是c(N2)=3mol/L,c(H2)=9mol/L,c(NH3)=4mol/L,求该温度时的平衡常数及N2、H2的起始浓度。
查看答案和解析>>
科目: 来源: 题型:
节能减排是构建社会主义和谐社会的重大举措。下列举措不符合这一要求的是
A.自2008年6月1日起,实行塑料购物袋有偿使用
B.包装盒、快餐盒等全部用聚苯乙烯生产,以减少木材的使用
C.农村大力发展沼气,将废弃的秸杆转化为清洁高效的能源
D.推广使用乙醇汽油作汽车燃料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com