
科目: 来源: 题型:
(1)在室温下测得0.1mol·L-1氨水PH=11,则该温度下氨水的电离度![]() =__________
=__________
(2)25℃时在0.1mol·L-1的H2A水溶液中,用氢氧化钠来调节溶液的pH,得到其中含H2A、HA-、A2-三种微粒的溶液。
①当溶液的pH=7时,c(Na+)=__________(填微粒间量的关系)
②当c(Na+)=c(A2-)+c(HA-)+c(H2A)时溶液为__________溶液(填物质)。
(3)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和液态水,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是__________。
(4)甲醇—空气燃料电池是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:2CH3OH+3O2=2CO2+4H2O。其工作原理示意图如下(其中a、b、c、d四个出入口表示通入或排出的物质)。

则负极的电极反应式为__________;正极的电极反应式为__________
查看答案和解析>>
科目: 来源: 题型:阅读理解
硫酸是重要的化工原料,二氧化硫生成三氧化硫是硫酸工业的重要反应之一。
(1)现将一定量的SO2(g)和O2(g)放入某固定体积的密闭容器中,在一定条件下,反应2SO2(g)+O2(g)![]() 2SO3(g)达到平衡状态。
2SO3(g)达到平衡状态。
①上述反应平衡常数的表达式K=__________
②能判断该反应达到平衡状态的标志是__________。(填字母)
a. SO2和SO3浓度相等 b. SO2百分含量保持不变
C. 容器中气体的压强不变 d. SO3的生成速率与SO2的消耗速率相等。
(2)某温度下,SO2的平衡转化率(![]() )与体系总压强(P)的关系如下图1所示。平衡状态由A变到B时,平衡常数K(A)__________K(B)(填“>”、“<”或“=”)。
)与体系总压强(P)的关系如下图1所示。平衡状态由A变到B时,平衡常数K(A)__________K(B)(填“>”、“<”或“=”)。
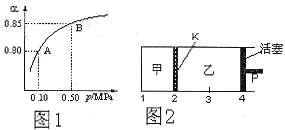
(3)如图2所示,保持温度不变,在一定反应条件下,将2molSO2和1molO2加入甲容器中,将4molSO2和2molO2加入乙容器中,隔板K不能移动。此时控制活塞P,使乙的容积为甲的2倍。
①若移动活塞P,使乙的容积和甲相等,达到新平衡时,SO3的体积分数甲__________乙。(填:“大于”、“小于”、或“等于”)
②若在甲容器中通入一定量的He气,使容器内的压强增大,则c(SO3)/c(SO2)将__________填:“增大”、“减小”、“不变”、“无法确定”)
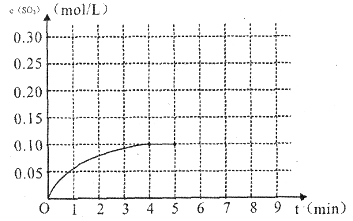
(4)将一定量的SO2(g)和O2(g)放入某固定体积的密闭容器中,在一定条件下,c(SO3)的变化如下图所示。若在第5分钟将容器的体积缩小一半后,在第8分钟达到新的平衡(此时SO3的浓度约为0.25mol/L)。请在下图中画出此变化过程中SO3浓度的变化曲线。
查看答案和解析>>
科目: 来源: 题型:
CoCl2![]() H2O在加热时会逐步失水,并呈现不同的颜色,实验室里可以制成变色硅胶,用以干燥并验证水份。以含钴废料(含少量Fe、Al等杂质)制取CoCl2
H2O在加热时会逐步失水,并呈现不同的颜色,实验室里可以制成变色硅胶,用以干燥并验证水份。以含钴废料(含少量Fe、Al等杂质)制取CoCl2![]() H2O的一种新工艺流程如下图:
H2O的一种新工艺流程如下图:
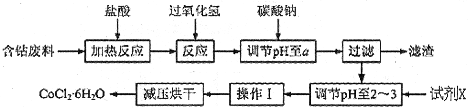
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2![]()
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
|
|
|
| 开始沉淀 | 2.3 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.2 | 5.2 |
请回答下列问题:
(1)写出加入过氧化氢时溶液中发生的离子反应方程式:__________
(2)加入碳酸钠调节pH至a,a的范围是__________;
(3)最合适的试剂X是__________
(4)操作I包含3个基本实验操作,它们是__________、__________和减压过滤。
(5)制得的CoCl2·6H2O需减压烘干的原因是__________。
查看答案和解析>>
科目: 来源: 题型:
实验和探究对化学学科的发展起着非常重要的作用
(1)写出下列实验过程中所体现的总的离子反应方程式:
①用PH试纸测得醋酸钠溶液呈碱性:__________
②用石墨做电极,电解硝酸银溶液后,溶液呈酸性:__________
③根据浑浊出现的快慢,探究硫代硫酸钠与酸反应速率的影响因素:__________
(2)已知锌能溶解在NaOH溶液中,产生H2。某同学据此设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S、质量为m1的镀锌铁皮与石墨用导线相连,放入6![]() NaOH溶液中,判断锌层完全反应的标志是:__________,最后,取出铁片用水冲洗、烘干后称量,得质量为m2,设锌镀层单侧厚度为h,锌的密度为
NaOH溶液中,判断锌层完全反应的标志是:__________,最后,取出铁片用水冲洗、烘干后称量,得质量为m2,设锌镀层单侧厚度为h,锌的密度为![]() ,则h=__________
,则h=__________
(3)实验室测定绿矾中FeSO4![]() 含量的步骤是:称1g绿矾,用30mL蒸馏水溶解并加入H2SO4溶液和H3PO4溶液,再用0.02mol/L KMnO4标准溶液滴定到溶液刚变成粉红色,停止滴定,消耗标准溶液VmL。反应中涉及的重要化学方程式有:
含量的步骤是:称1g绿矾,用30mL蒸馏水溶解并加入H2SO4溶液和H3PO4溶液,再用0.02mol/L KMnO4标准溶液滴定到溶液刚变成粉红色,停止滴定,消耗标准溶液VmL。反应中涉及的重要化学方程式有:
![]()
![]()
①绿矾的含量为__________%。
②![]() 的作用是__________。
的作用是__________。
查看答案和解析>>
科目: 来源: 题型:
下列关于溶液中的描述正确的是
A. 常温时,![]() 溶液的
溶液的![]() ,则该溶液中
,则该溶液中![]()
B. ![]() 溶液与
溶液与![]() 溶液反应至中性的离子方程式为:
溶液反应至中性的离子方程式为:
![]()
C. 常温下物质的量浓度相等的下列四种溶液:①![]() ;②
;②![]() ;③
;③![]() ;④
;④![]() ,四种溶液中
,四种溶液中![]() 比较:②
比较:②![]() ①
①![]() ④
④![]() ③
③
D. 常温下![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]() 可以常量共存
可以常量共存
查看答案和解析>>
科目: 来源: 题型:
锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:![]() =
=![]()
![]() ,下列说法错误的是
,下列说法错误的是
A. 电池工作时,锌失去电子
B. 电池正极的电极反应式为:![]()
C. 电池工作时,电子由正极通过外电路流向负极
D. 外电路中每通过![]() 电子,锌的质量理论上减少
电子,锌的质量理论上减少![]()
查看答案和解析>>
科目: 来源: 题型:
下列事实中,不能用勒夏特列原理解释的是
A. 溴水中有下列平衡![]()
![]()
![]() ,当加入
,当加入![]() 溶液后,溶液颜色变浅
溶液后,溶液颜色变浅
B. 对![]()
![]()
![]() 平衡体系,增大平衡体系的压强可使颜色变深
平衡体系,增大平衡体系的压强可使颜色变深
C. 反应![]()
![]()
![]() (正反应放热),升高温度可使平衡向逆反应方向移动
(正反应放热),升高温度可使平衡向逆反应方向移动
D. 打开啤酒瓶盖后产生大量的气泡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com