
科目: 来源: 题型:
下列说法不正确的是
A.已知4HC1(g)+O2(g)=2H2O(g)+2C12(g)能自发进行,则该反应:△H<0,△S<0
B.常温下0.1mol·L-1CH3COOH的pH为2.88,可以说明CH3COOH为弱电解质
C.其他条件不变,增大压强,平衡可能移动,但平衡常数一定不变
D.铁制品的表面镶锌块和铁制品表面镀锡,都能起到防腐的作用,且防腐原理是相同的
查看答案和解析>>
科目: 来源: 题型:
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+===2As+3SnCl![]() +6M,关于该反应的说法中正确的组合是 ( )
+6M,关于该反应的说法中正确的组合是 ( )
①氧化剂是H3AsO3 ②还原性:Cl->As ③每生成7.5 g As,还原剂失去的电子为0.3 mol ④M为OH- ⑤SnCl![]() 是氧化产物
是氧化产物
A.①③⑤ B.①②④⑤
C.①②③④ D.①③
查看答案和解析>>
科目: 来源: 题型:
含有a mol FeBr2的溶液中,通入x mol Cl2.下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是 ( )
A.x=0.4a,2Fe2++Cl2===2Fe3++2Cl-
B.x=0.6a,2Br-+Cl2===Br2+2Cl-
C.x=a,2Fe2++2Br-+2Cl2===Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2===2Br2+2Fe3++6Cl-
查看答案和解析>>
科目: 来源: 题型:
下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是( )
A.Ba2+ 、NO3-、NH4+、Cl- B. Ca2+、HCO3-、NH4+、AlO2-
C.K+、Ba2+、Cl-、HSO3- D. Mg2+ 、NH4+、SO42-、K+
查看答案和解析>>
科目: 来源: 题型:
下列方程式正确的是( )
A.硫酸氢钠溶液中加入氢氧化钡溶液至溶液pH=7:Ba2+ + SO42-= BaSO4↓
B.硫化钠溶液显碱性的原因:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
C.等体积、等浓度的Ca(HCO3)2溶液和NaOH溶液混合Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
D.氧化亚铁溶于稀硝酸中:3FeO+NO3-+10H+=3Fe3++NO↑+5H2O
查看答案和解析>>
科目: 来源: 题型:
下列离子组在指定溶液中一定能大量共存的是
A.c(I-)=0.1 mol·L-1的溶液中: Na+、Fe3+、ClO-、SO42-
B.由水电离产生的c(OH-)=1×10-10 mol·L-1的溶液中:Ba2+、K+、NO3-、Br-
C.0.2 mol·L-1NaHC2O4溶液中:Ca2+、Na+、OH-、Cl-
D.加入Al能放出H2的溶液中:K+、NH4+、NO3-、Cl-
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.在由水电离产生的氢离子浓度为10-13 mol•L—1的溶液中,Ca2+、K+、Cl-、HCO3-
四种离子能大量共存
B.常温下,将0.2 mol•L-1某一元碱ROH溶液和0.1 mol•L-1HCl溶液等体积混合,
混合后溶液pH<7,则c(ROH)>c(R+)
C.反应2N2H4(l)=N2(g)+2H2(g)△H=-50.6 kJ /mol,只在高温下自发进行
D.已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有
c(Mg2+)=c(CO32-) ,且c(Mg2+)·c(CO32-)=6.82×10-6
查看答案和解析>>
科目: 来源: 题型:
两种硫酸盐按一定比例混合后共熔,可制得化合物X且X溶于水能电离出K+、Cr3+、SO42-,若将2.83 g X中的Cr3+全部氧化为Cr2O72-后,溶液中的Cr2O72-可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为:Cr2O72-+6I-+14H+=2 Cr3++3I2+7H2O 。若向溶有2.83 gX的溶液中,加入过量的BaCl2溶液,可得到4.66 g白色沉淀.由此可推断出X的化学式为
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
关于下列各图的叙述中正确的是
 | |||
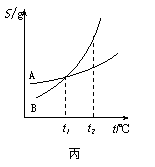 | 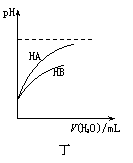 | ||
A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ·mol-1
B.乙表示恒温恒容条件下,2NO2(g)![]() N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将tl℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH
查看答案和解析>>
科目: 来源: 题型:
硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、漂白粉等一系列物质(见下图)。下列说法正确的是

A.CO、SO2、SO3均是酸性氧化物
B.除去与水反应,图示转化反应均为氧化还原反应
C.工业上利用Cl2和澄清石灰水反应来制取漂白粉
D.用CO合成CH3OH进而合成HCHO的两步反应,原子利用率均为100%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com