
科目: 来源: 题型:
能使H2O![]() H++OH-电离平衡向正反应方向移动,而且所得溶液显酸性的是( )
H++OH-电离平衡向正反应方向移动,而且所得溶液显酸性的是( )
A、将水加热到99℃,使水的pH=6.1 B、在水中滴入稀硫酸
C、在水中加入小苏打 D、在水中加入氯化铝固体
查看答案和解析>>
科目: 来源: 题型:
可逆反应①X(g)+2Y(g)![]() 2Z(g)、②2M(g)
2Z(g)、②2M(g)![]() N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:

下列判断正确的是( )
A.反应①的正反应是吸热反应
B.达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为14∶15
C.达平衡(Ⅰ)时,X的转化率为![]()
D.在平衡(Ⅰ)和平衡(Ⅱ)中,M的体积分数相等
查看答案和解析>>
科目: 来源: 题型:
某温度下,H2(g)+CO2(g)![]() H2O(g)+CO(g)的平衡常数K=
H2O(g)+CO(g)的平衡常数K=![]() 。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
下列判断不正确的是( )
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目: 来源: 题型:
1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大大满足了当时日益增长的人口对粮食的需求。下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是( )
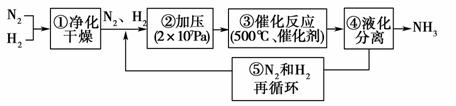
A.①②③ B.②④⑤
C.①③⑤ D.②③④
查看答案和解析>>
科目: 来源: 题型:
一定条件下,对于可逆反应X(g)+3Y(g)2Z(g),若X、Y、Z的起始浓度分别为 c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是( )
A.c1∶c2=3∶1 B.平衡时,Y和Z的生成速率之比为2∶3
C.X、Y的转化率相等 D.c1的取值范围为0.04 mol/L<c1<0.14 mol/L
查看答案和解析>>
科目: 来源: 题型:
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体 ②H2O ③NH4Cl固体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
A、②④⑥ B、①② C、②③⑤ D、②④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
α1和α2分别为A在甲、乙两个恒容容器中平衡体系A(g)![]() 2B(g)和2A(g)
2B(g)和2A(g)![]() C(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是( )
C(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是( )
A.α1、α2均减小 B.α1、α2均增大
C.α1减小,α2增大 D.α1增大,α2减小
查看答案和解析>>
科目: 来源: 题型:
在一定条件下,向2 L恒容密闭容器中加入2 mol X、1 mol Y。发生如下反应:2X(g)+Y![]() 3Z(g);ΔH=-a kJ·mol-1(a>0)。经60 s达平衡,此时Y的物质的量为0.2 mol。下列说法错误的是( )
3Z(g);ΔH=-a kJ·mol-1(a>0)。经60 s达平衡,此时Y的物质的量为0.2 mol。下列说法错误的是( )
A.用Z表示的化学反应速率为1.2 mol·L-1·min-1
B.若再充入1 mol Z,重新达到平衡时,X的体积分数不变,则Y为气态
C.达平衡后,实际放出的热量为b kJ,则b=a
D.若Y为气态,则使容器体积变为1 L,Z的物质的量不会增大
查看答案和解析>>
科目: 来源: 题型:
图中的曲线是表示其他条件一定时,2NO+O22NO2 ΔH<0反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v正>v逆的点是( )
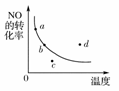
A.a点 B.b点 C.c点 D.d点
查看答案和解析>>
科目: 来源: 题型:
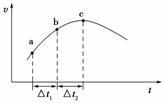
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)![]() SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下图所示。由图可得出的正确结论是( )
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下图所示。由图可得出的正确结论是( )
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应物的总能量低于生成物的总能量
D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com