
科目: 来源: 题型:
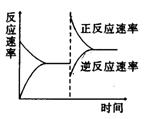
右图是关于反应A2(g)+3B2(g) ![]() 2C(g) △H<0的平衡移动图形,影响平衡移动的原因是
2C(g) △H<0的平衡移动图形,影响平衡移动的原因是
A、升高温度,同时加压。
B、降低温度,同时减压
C、增大反应物浓度,同时减小生成物浓度
D、增大反应物浓度,同时使用催化剂;
查看答案和解析>>
科目: 来源: 题型:
下列措施或事实不能用勒夏特列原理解释的是
A.新制的氯水在光照下颜色变浅
B.Fe(SCN)3溶液中加入6mol/L NaOH溶液后颜色变浅
C.在合成氨的反应中,降温或加压有利于氨的合成
D.H2、I2、HI平衡混合气加压后颜色变深
查看答案和解析>>
科目: 来源: 题型:
一定条件下,在2SO2+O2 ![]() 2SO3的化学平衡体系中,各物质的浓度分别是2.0mol/L、0.8mol/L、2.4mol/L则氧气在起始的浓度可能是
2SO3的化学平衡体系中,各物质的浓度分别是2.0mol/L、0.8mol/L、2.4mol/L则氧气在起始的浓度可能是
A. 0~0.8mol/L B. 0.8~2 mol/L C. 0~2 mol/L D. 无法确定
查看答案和解析>>
科目: 来源: 题型:
下列反应中,熵减小的是
A、(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) B、2N2O5(g)=4NO2(g)+O2(g)
C、 MgCO3(s)=MgO(s)+CO2(g) D、2CO(g)=2C(s)+O2(g)
查看答案和解析>>
科目: 来源: 题型:
2A(g)+B(g) ![]() 3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是
3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是
A.V(A)=0.7mol.L-1.min-1 B.V(B)=0.3mol.L-1.min-1
C.V(C)=0.9mol.L-1.min-1 D.V(D)=1.1mol.L-1.min-1
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式中,△H能表示对应物质的标准燃烧热的是
A.2C8H18O(l)+25O2(g)==16CO2(g)+18H2O(l) △H =-11828.0 kJ•mol—1
B.CO(g)+![]() O2(g)==CO2(g) △H = -283.0 kJ•mol—1
O2(g)==CO2(g) △H = -283.0 kJ•mol—1
C.C(s)+ ![]() O2(g)==CO(g) △H = -110.5 kJ•mol—1
O2(g)==CO(g) △H = -110.5 kJ•mol—1
D.H2(g)+ ![]() O2(g)==H2O(g) △H = -241.8 kJ•mol—1
O2(g)==H2O(g) △H = -241.8 kJ•mol—1
查看答案和解析>>
科目: 来源: 题型:
强酸与强碱的稀溶液发生中和反应的热效应: H+(aq)+OH-(aq)=H2O(1);
ΔH =-57.3kJ/mol。向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应ΔH 1、ΔH 2、ΔH 3的关系正确的是
A.ΔH 1>ΔH 3>ΔH 2 B.ΔH 1>ΔH 2>ΔH 3
C.ΔH 1<ΔH 3<ΔH 2 D.ΔH 1<ΔH 2<ΔH 3
查看答案和解析>>
科目: 来源: 题型:
相同温度下,有下列三个热化学方程式:
(1)2H2(l)+O2(g)=== 2H2O(l) △H1= -Q1 kJ• mol-1
(2)2H2(g)+O2(g)=== 2H2O(l) △H1= -Q2 kJ• mol-1
(3)2H2(l)+O2(g)=== 2H2O(g) △H1= -Q3 kJ• mol-1
则Q1、Q2、Q3的关系表示正确的是( )
A.Q1=Q2 =Q3 B. Q1=Q2<Q3 C.Q2 > Q1 >Q3 D.Q3> Q2> Q1
查看答案和解析>>
科目: 来源: 题型:
根据热化学方程式(在101 kPa时):S(s)+O2(g)===SO2(g)ΔH=-297.23 kJ/mol,分析下列说法中不正确的是 ( )
A.S的燃烧热为297.23 kJ/mol
B.形成1 mol SO2的化学键所释放的总能量大于断裂1 mol S(s)和1 mol O2(g)的化学键所吸收的总能量
C.S(g)+O2(g)===SO2(g)放出的热量小于297.23 kJ
D.S(g)+O2(g)===SO2(g)放出的热量大于297.23 kJ
查看答案和解析>>
科目: 来源: 题型:
下列变化过程,属于放热过程的是( )
①液态水变成水蒸气 ②酸碱中和反应 ③浓H2SO4稀释 ④固体氢氧化钠溶于水 ⑤H2在Cl2中燃烧 ⑥弱酸电离 ⑦NH4Cl晶体与Ba(OH)2·8H2O混合搅拌
A.①③⑤ B.①⑥⑦ C.②③④ D.②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com