
科目: 来源: 题型:
下列说法中不正确的是( )
A.不需要加热就能发生的发应一定是放热反应
B.吸热反应在常温下可能发生
C.反应吸热还是放热,取决于反应物和生成物所具有的总能量的相对大小
D.物质发生化学变化一定伴随着能量变化
查看答案和解析>>
科目: 来源: 题型:
将含有C、H、O的芳香族化合物3.24 g,装入元素分析装置,通入足量的O2使它完全燃烧,将生成的气体依次通过氯化钙干燥管A和碱石灰干燥管B。测得A管质量增加了2.16g,B管增加了9.24g。已知该有机物的相对分子质量为108。
⑴燃烧此化合物3.24g,须消耗氧气的质量是多少?
⑵求此化合物的分子式?ks5u
⑶该化合物1H核磁共振谱上有5个信号峰,试写出符合的结构简式。
查看答案和解析>>
科目: 来源: 题型:
在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g)+B(g) ![]() xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于________________
(2)A的转化率为_________________
(3)生成D的反应速率为_________________
(4)如果增大反应体系的压强,则平衡体系中C的质量分数_________(填变大、变小、不变)
(5)如果上述反应在相同条件下从逆反应开始进行,开始加入C和D各![]() mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入________物质_________mol
mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入________物质_________mol
查看答案和解析>>
科目: 来源: 题型:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解5mol水消耗的能量是_____________kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____________;
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对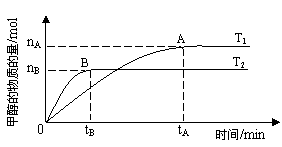 反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
下列说法正确的是________(填序号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为:v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
②该反应为放热反应
③该反应在T1时的平衡常数比T2时的小
④处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为______;
查看答案和解析>>
科目: 来源: 题型:
物质A~Z有下图所示的转化关系(部分反应物与产物已略去)。其中,常温下B、C为气体单质,Y为固体单质,Y是电子工业中常用的半导体材料。F是具有磁性的黑色晶体。E的水溶液与M混合后得到N,N经过干燥脱水可得到一种常用于实验室和袋装食品、瓶装食品等的干燥剂,K的焰色反应为紫色,A的焰色反应为黄色。

请回答:
(1)利用①反应进行化工生产的工业名称为 ,K的化学式 ;D的电子式________________;
(2)反应①的离子方程式 ;
(3)向H的水溶液中加入足量氨水并将溶液露置在空气中,观察到的现象是 ;向相同体积相同浓度的两份G溶液中分别滴加相同PH的氨水和D溶液,当沉淀最大量时所加入的氨水和D溶液的体积分别为V1、V2,则V1、V2的大小关系V1 V2。
(4)写出反应⑥的化学方程式 。
(5)N为比碳酸还弱的酸,设计实验证明,简述实验过程和现象 。
查看答案和解析>>
科目: 来源: 题型:
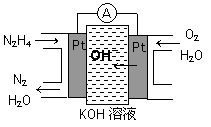
肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用氧化剂。试回答下列问题
(1)肼燃料电池原理如图所示,左边电极上发生的电极反应式为_________。
(2)火箭常用N2O4作氧化剂,肼作燃料,已知:
N2(g)+2O2(g)=2NO2(g) △H =-67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-534.0kJ·mol-1
2NO2(g)![]() N2O4(g) △H =-52.7kJ·mol-1
N2O4(g) △H =-52.7kJ·mol-1
试写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方________。
(3)联氨的工业生产常用氨和次氯酸钠为原料获得,写出反应的离子方程式为_ __。
(4)如图所示,A是由易导热材料制成的体积不变的密闭容器,B是一耐化学腐蚀且易于传热的体积可变的透明气囊(体积改变过程中囊体弹力改变忽略不计)。关闭K2,将各1 mol NO2通过K1、K3分别充入A、B中,反应起始时A、B的体积相同均为a L。
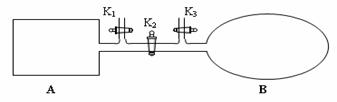
①B中可通过________________判断可逆反应2NO2![]() N2O4已经达到平衡。
N2O4已经达到平衡。
②若打开K2,平衡后B容器的体积缩至0.4a L,则打开K2之前,气球B体积为______L。
③若容器A中到达平衡所需时间t s,达到平衡后容器内压强为起始压强的0.8倍,则 平均化学反应速率v(NO2)等于____________________(用含a、t的代数式表示)。
④若平衡后在A容器中再充入0.5mol NO2,则重新到达平衡后,平衡混合气中NO2的体积分数_______________(填 “变大”“变小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
某气态不饱和链烃CmHn 在镍的催化下跟氢气发生加成反应,生成产物CmHn+x。今取CmHn与氢气的混合气体共60 mL进行实验,反应前混合气体中氢气体积为W(横坐标),反应后气体总体积为V(纵坐标),其相互关系如图所示:上述气体的体积均是在同温同压下测定,单位是mL。由此可知x的数据是( )
A.2 B.3 C.4 D.5
查看答案和解析>>
科目: 来源: 题型:
由乙烯,环丙烷,乙醛(C2H4O)组成的混合物,经测定其中碳元素的质量分数为72%,则混合物中,氧元素的质量分数为 ( )
A. 32% B. 22.65% C. 16% D. 2.14%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com