
科目: 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.1 mol Fe2+被足量的H2O2溶液氧化,转移2NA个电子
B.1 L 0.1 mol·L-1氨水含有0.1NA个OH-
C.1molFeCl3与沸水反应生成NA个Fe(OH)3胶粒
D.常温下,23 g NO2含有NA个氧原子
查看答案和解析>>
科目: 来源: 题型:
在电解质溶液的导电性实验(装置如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是
A.盐酸中逐滴加入氢氧化钠溶液
B.硫酸铜溶液中逐滴加入氢氧化钡溶液
C.硫酸中逐滴加入氨水
D.盐酸中逐滴加入硝酸银溶液

查看答案和解析>>
科目: 来源: 题型:
下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是
A.Cu(OH)2与盐酸,Cu(OH)2与醋酸
B.BaCl2溶液与Na2SO4溶液,Ba(OH)2溶液与H2SO4溶液
C.NaHCO3溶液与NaHSO4溶液,NaHCO3溶液与盐酸
D.石灰石与稀硝酸反应,生石灰与稀盐酸
查看答案和解析>>
科目: 来源: 题型:
科学的分类方法可提高学习效率,以达到事半功倍的效果。下列分类标准合理的是
①根据氧化物的元素组成将氧化物分为金属氧化物和非金属氧化物②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 ③根据分散系是否有丁达尔效应来区分溶液、胶体 ④根据物质溶于水或熔化状态是否导电分为电解质和非电解质
A.①②④ B.①② C.①②③ D.①②③④
查看答案和解析>>
科目: 来源: 题型:
用下图表示的一些物质或概念之间的从属或包含关系中不正确的是
| X | Y | Z | |
| A | 含氧酸 | 酸 | 化合物 |
| B | 胶体 | 分散系 | 混合物 |
| C | 电解质 | 化合物 | 纯净物 |
| D | 置换反应 | 氧化还原反应 | 离子反应 |

查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | ||||||||||||||||
 试回答下列问题:
试回答下列问题:
(1)请写出字母O代表的元素符号 ,该元素在周期表中的位置 。
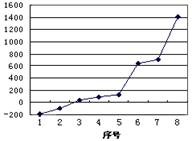
(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号)。
(3)由j原子跟c原子以1 : 1相互交替结合而形成的晶体,晶型与晶体j相同。两者相比熔点更高的是 (填化学式),试从结构角度加以解释: 。
(4)k与l形成的化合物kl2的电子式是 ,它在常温下呈液态,形成晶体时,属于 晶体。
(5)i单质晶体中原子的堆积方式如下图(甲)所示,其晶胞特征如下图(乙)所示,原子之间相互位置关系的平面图如下图(丙)所示。

若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
一个晶胞中i原子的数目为 , 该晶体的密度_ (用M、NA、d表示)。
(6)a与d构成的阳离子和i的阳离子可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加人浓氢氧化钡溶液,产生的现象有:①.溶液中出现白色沉淀并伴有有刺激性气味气体放出,②.沉淀逐渐增多后又逐渐减少直至最终沉淀的量不变。写出沉淀的量不变时发生反应的离子方程式__________ __ __________。
查看答案和解析>>
科目: 来源: 题型:
工业上以氯化钾和钛白厂的副产品硫酸亚铁为原料可得到硫酸钾、过二硫酸钠和铁红颜料等产品,该方法原料的综合利用率较高。
(1)基态钛原子的核外电子排布式为 。
(2)TiCl4在常温下是一种无色液体,而FeCl3可用升华法提纯,则两种氯化物均属于
晶体。
(3)SO42-和 S2O82-(过二硫酸根)结构中,硫原子均位于由氧原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构。下列说法正确的是 。
A.SO42-中存在σ键和π键且与PO43-离子互为等电子体
B.S2O82-中存在非极性键且有强氧化性
C.S2O82-比SO42- 稳定且两者的氧元素的化合价相同
(4)KCl与MgO的晶体结构跟NaCl的晶体结构相似,则KCl与MgO两者中熔点高的是 ,原因是 。
(5)硫与氯可形成化合物SCl2,则该分子中硫原子的杂化方式为 ,分子的空间构型为 。
(6)在一定条件下铁形成的晶体的基本结构单元如下图1和图2所示,则图1和图2的结构中铁原子的配位数之比为 。
 |
查看答案和解析>>
科目: 来源: 题型:阅读理解
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
(1)某同学根据上述信息,推断B的核外电子排布如右图所示 ,
,
该同学所画的电子排布图违背了 。
(2)根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为 。
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确 (填是、否),并阐述理由 。

 (4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物, 其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式 ,该物质的K原子和C60分子的个数比为 。
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物, 其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的价电子排布式 ,该物质的K原子和C60分子的个数比为 。
(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为 。
(6) 晶体硼的基本结构单元是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,试观察图形回答:这个基本结构单元由_____个硼原子组成,共含有________个B-B键。
查看答案和解析>>
科目: 来源: 题型:
I、 卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1) ①HClO4、②HIO4、③H5IO6 的酸性由强到弱的顺序为 (填序号)。
(2)卤素互化物如BrI、ICl等与卤素单质结构相似、性质相近。Cl2、BrI、ICl沸点由高到低的顺序为_________。
(3)气态氟化氢中存在二聚分子(HF)2,这是由于 。
(4)I3+(可看成II2+)属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为 。
(5)卤化物RbICl2加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式为 。
II.氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
⑴ 出N2H62+在足量碱性溶液中反应的离子方程式 。
⑵NH2-的电子式为 。
(3)写出两种由多个原子组成的含有与N3-电子数相同的物质的化学式 。
(4)等电子数的微粒往往具有相似的结构,试预测N3—的构型 。
(5)据报道,美国科学家1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片 所带电荷是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com