
科目: 来源: 题型:
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)合成氨反应 ,在2 L密闭容器中通入2 mol的N2和6 mol的H2,5 min时反应达到平衡,此时容器内的压强变为原来的3/4,0—5min该反应的化学反应速率为V(H2)= ,N2的转化率= ,化学平衡常数K= 。
(2)NH3 (g)与CO2(g)经过两步反应生成尿素〔CO(NH2)2〕,两步反应的能量变化示意图如下:

则NH3(g) 与CO2(g) 反应生成尿素的热化学方程式为 。
(3)用CO合成甲醇(CH3OH)的化学方程式为![]() ,
,
 按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右下图所示。下列说法正确的是 (填字母)
按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右下图所示。下列说法正确的是 (填字母)
A.温度:T1 > T2 > T3
![]() B.平衡常数:
B.平衡常数:
![]() C.平衡常数:
C.平衡常数:
![]() D.正反应速率:
D.正反应速率:
![]() E. 平均摩尔质量:
E. 平均摩尔质量:
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中C(NH+4)=C(Cl?),则溶液显( )性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb= 。
查看答案和解析>>
科目: 来源: 题型:
为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3)。
CCl4+H2 ![]() CHCl3+HCl 此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等。已知CCl4的沸点为 77℃,CHCl3的沸点为 61.2℃。(1)在密闭容器中,该反应在某催化剂下进行10 h,测得如下数据(假设不考虑副反应)。
CHCl3+HCl 此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等。已知CCl4的沸点为 77℃,CHCl3的沸点为 61.2℃。(1)在密闭容器中,该反应在某催化剂下进行10 h,测得如下数据(假设不考虑副反应)。
| 实验序号 | 温度℃ | 初始CCl4浓度(mol·L-1) | 初始H2浓度(mol·L-1) | CCl4的转化率 |
| 1 | 110 | 0.8 | 1.2 | A |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 100 | 1 | 1 | B |
①此反应的化学平衡常数表达式为 ,在 110 ℃时平衡常数为 。
②实验1中,CCl4的转化率A 50%(填“大于”、“小于”或“等于”)。
③实验2中,10h后达到平衡,H2的平均反应速率为 。在此实验的平 衡体系中,再加入0.5 mol CCl4和1.0 mol HCl,平衡将向 方向移动。
④实验3中,B的值 (选填序号)。
A.等于50% B.大于50% C.小于50% D.从本题资料,无法判断
查看答案和解析>>
科目: 来源: 题型:
在某温度下的水溶液中,c(H+)=10x mol·L-1,c(OH-)=10ymol·L-1,x与y关系如图所示。
(1)该温度下,0.01 mol·L-1NaOH溶液的pH为________。
 (2)在此温度下,将pH=13的NaOH溶液Va L与pH=1的
(2)在此温度下,将pH=13的NaOH溶液Va L与pH=1的
硫酸溶液Vb L混合。
①若所得混合液为中性,则Va∶Vb=________。
②若所得混合液的pH=2,则Va∶Vb=________。
查看答案和解析>>
科目: 来源: 题型:
实验室中有一未知浓度的稀盐酸,某学生在实验室中进行测定盐酸浓度的实验,请完成下列填空:
(1)配制100 mL 0.10 mol/L NaOH标准溶液。
(2)取20.00 mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
| 滴定次数 | 待测盐酸的体积(mL) | 标准NaOH溶液体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 20.00 | 0.40 | 20.50 |
| 第二次 | 20.00 | 4.10 | 24.00 |
| 第三次 | 20.00 | 1.00 | 24.00 |
①滴定达到终点的现象是 。此时锥形瓶内溶液的pH范围为 。
②根据上述数据,可计算出该盐酸的浓度约为___________ mol/L(保留小数点后二位数)。
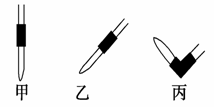
③排去碱式滴定管中气泡的方法应采用下图操作________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有__________。
 A.滴定终点读数时俯视读
A.滴定终点读数时俯视读
B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥
D.称量NaOH固体中混有Na2CO3固体
E.碱式滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目: 来源: 题型:
常温下有浓度均为0.1mol·L-1的四种溶液:①碳酸钠溶液;②碳酸氢钠溶液;③盐酸;④氨水。请根据题目要求回答下列问题。
(1) 上述溶液中,既能与氢氧化钠溶液反应,又能与硫酸溶液反应的是__________。
(2) 取适量溶液④,加入少量氯化铵固体,此时溶液中 ![]() 的值_____(填“增大” 或“减小”或“不变”)。
的值_____(填“增大” 或“减小”或“不变”)。
(3) 将等体积的③和④的溶液混合后,所得溶液中离子浓度由大到小的顺序是:__________。 所得溶液的pH<7,用离子方程式表示其原因________________;混合后的溶液中由水电 离
出的c(OH-)____0.1 mol/L NaOH溶液中由水电离出的c(OH-) (填“>”、“<”或“=”)。
(4) 取10mL溶液③,加水稀释到500mL,则该溶液中由水电离出c(H+)=________________。
(5) 若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子物质的量浓度由大到小的关系是__________。
(6) 有相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.CH3COONH4;C.(NH4)2SO4; D.NH4Cl, 按pH由大到小的顺序排列_______ _(填序号)
查看答案和解析>>
科目: 来源: 题型:
草酸(H2C2O4)是二元弱酸,草酸氢钾溶液呈酸性。在常温下10mLpH=10 的KOH溶液中,加入pH=4的H2C2O4溶液至pH刚好等于7(假设反应前后体积不变),则对反应后溶液的叙述正确的是( )
A. C(K+)+C(H+)=C(HC2O4¯)+C(OH¯)+ C(C2O42-) B. C(K+)=C(HC2O4¯)+2C(C2O42-)
C. C(K+)= C(H2C2O4)+C(HC2O4¯)+ C(C2O42-) D. V总≧20mL
查看答案和解析>>
科目: 来源: 题型:
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)![]() I3-(aq), 某I2、KI混合溶液中, c(I3-)与温度T的关系如下图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
I3-(aq), 某I2、KI混合溶液中, c(I3-)与温度T的关系如下图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
A.反应 I2(aq)+I-(aq)![]() I3-(aq) ΔH>0
I3-(aq) ΔH>0
B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K2>K1
C.若T1时,反应进行到状态d时,一定有υ正>υ逆
D.状态a与状态b相比,状态b时I2的转化率更高

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com