
科目: 来源: 题型:
A、B、C、D四种强电解质溶液分别含有下列阴、阳离子中的各一种且不重复:NH+4、 Ba2+、Na+、H+、SO2-4、NO—3、OH—、CO2-3
已知:①向A或D中滴入C,均有沉淀生成:
②向A和B中分别滴加D(可加热)均有气体生成,且这两种气体在水中能反应生成D。 试回答下列问题:
(1)写出A、B、C、D四种溶液中溶质的化学式:
A ,B ,C ,D 。
(2)D和B反应生成气体,该气体能被足量的A吸收,写出该过程中发生反应的离子方程式 。
(3)将A与D反应生成的气体缓慢通入含KOH、Ca(OH)2、NaA1O2的混合溶液中,生成沉淀的物质的量n与通入气体的体积V的关系可表示为 (填字母)。

查看答案和解析>>
科目: 来源: 题型:
金属铝在酸性或碱性溶液中均可与NO3-发生氧化还原反应,转化关系如下:
 |
已知,气体D和F反应可生成盐,气体D和A溶液反应生成白色沉淀。
请回答下列问题:
(1) A和B两溶液混合产生白色沉淀,该白色沉淀的化学式
(2) C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C、E转化为无毒的气态单质,该单质的电子式
(3)完成铝在碱性条件下与NO3-反应的离子方程式 。
(4)除去气体C中的杂质气体E的化学方法: (用化学方程式表示)
(5)Al与NO3-在酸性条件下反应,Al与被还原的NO3-的物质的量之比是 。
查看答案和解析>>
科目: 来源: 题型:
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:

(1)④、⑤、⑥的离子半径由大到小的顺序为_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
a.MnO2 b.KMnO4 c.Na2SO3 d. FeCl 3
(5)由表中元素形成的物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为_____________________,
常温下,为使0.1 mol/L M溶液中M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至_________________。
查看答案和解析>>
科目: 来源: 题型:
某溶液中可能含有OH—、CO32—、AlO2—、SiO32—、SO42—、Na+、Fe3+、Mg2+、Al3+等离![]() 子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如下图所示。下列说法正确的是
子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如下图所示。下列说法正确的是
A.原溶液中一定含有的阴离子是:OH-、SiO32-、AlO2-、CO32-
B.反应最后形成的溶液中的溶质为NaCl
C.原溶液中一定含有Na2SO4
D.原溶液中含有CO32-与AlO2-的物质的量之比为1:1

查看答案和解析>>
科目: 来源: 题型:
海洋约占地球表面积的71%,对其进行开发利用的部分流程如下图所示。下列说法
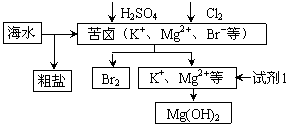 不正确的是
不正确的是
A.可用BaCl2溶液除去粗盐中的SO42-
B.从苦卤中提取Br2的反应的离子方
程式为:2Br— + Cl2 == 2Cl— + Br2
C.试剂1可以选用石灰乳
D.工业上,电解熔融Mg(OH)2冶炼金属镁
查看答案和解析>>
科目: 来源: 题型:
A是一种常见单质,B、C为常见化合物,A、B、C均含有元素X,它们有如图的转化
关系(部分产物及反应条件已略去)。下列判断正确的是
A.X元素可能为Al
B.X元素一定为金属元素
C.反应①和②一定互为可逆反应
D.反应①和②一定为氧化还原反应

查看答案和解析>>
科目: 来源: 题型:
将磁性氧化铁放入稀HNO3中,可发生如下反应:
3Fe3O4 +28HNO3 = 9Fe(NO3)X + NO↑+14H2O,下列判断合理的是
A.Fe(NO3)X中的X为2
B.稀HNO3在反应中只表现氧化性
C.反应中每还原0.4mol氧化剂,就有1.2mol电子转移
D.磁性氧化铁中的所有铁元素全部被氧化
查看答案和解析>>
科目: 来源: 题型:
在T℃时,将a g NH3完全溶于水,得到VmL溶液,假设该溶液的密度为ρg·cm-3,溶质的质量分数为w,其中含NH+4的物质的量为b mol。下列叙述中正确的是
A.溶质的质量分数为![]()
B.溶质的物质的量浓度![]()
C.溶液中![]()
D.上述溶液中再加入VmL水后,所得溶液溶质的质量分数大于0.5w
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写不正确的是
A.NaOH溶液与SO2反应,当n(NaOH):n(SO2) =4:3时:
4OH—+3SO2= SO2—3+ 2HSO—3+ H2O
B.酸性条件下KIO3溶液与KI溶液发生反应生成I2:![]()
C.AgNO3溶液中加入过量的氨水:![]()
D.1 mol·L-1的NaAlO2溶液和2.5 mol·L-l的HC1等体积互相均匀混合:
![]()
查看答案和解析>>
科目: 来源: 题型:
实验室需配制一种仅含五种离子(水电离出的离子可忽略)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为1 mol/L,下面四个选项中能达到此目的的是
A.Ca2+、K+、OH—、Cl—、NO—3 B.Fe2+、H+、Br—、NO—3、Cl—
C.Na+、K+、SO2—4、NO—3、Cl— D.Al3+、Na+、Cl—、SO2-4、NO—3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com