
科目: 来源: 题型:
已知反应:
①101kPa时,2C(s) +O2(g)==2CO(g);ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OHˉ(aq)==H2O(l);ΔH=-57.3 kJ/mol。下列结论正确的是( )
A.碳的燃烧热小于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出的热量小于57.3 kJ
查看答案和解析>>
科目: 来源: 题型:
已知在1.01×105Pa、298K条件下,2mol 氢气在氧气中燃烧生成水蒸气放出484kJ热量。下列热化学方程式正确的是( )
A.H2O(g) === H2(g)+![]() O2(g) △H= +242kJ·mol-1
O2(g) △H= +242kJ·mol-1
B.2H2(g)+O2(g)===2H2O(l) △H= -484kJ·mol-1
C.H2(g)+![]() O2(g)===H2O(g) △H= +242kJ·mol-1
O2(g)===H2O(g) △H= +242kJ·mol-1
D.2H2(g)+O2(g)===2H2O(g) △H= +484kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
下列有关热化学方程式的叙述中,正确的是( )
A.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则表示该反应中和热的热化学方程式为 NaOH(aq)+HCl(aq) ===NaCl(aq)+H2O(l) ΔH=+57.4 kJ/mol
B.已知C(石墨,s) ===C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C.已知2H2(g)+O2(g) ===2H2O(g) ΔH=-483.6 kJ/mol,则H2燃烧热为241.8 kJ/mol
D.已知2C(s)+2O2(g) ===2CO2(g) ΔH1,;2C(s)+O2(g) ===2CO(g) ΔH2;则ΔH1<ΔH2
查看答案和解析>>
科目: 来源: 题型:
有一硫酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到6.99g的沉淀;滤液与2.0 mol·L-1 NaOH溶液反应,用去35mL碱液时恰好完全中和。试求混合液中H2SO4、HNO3的物质的量浓度各是多少?
查看答案和解析>>
科目: 来源: 题型:
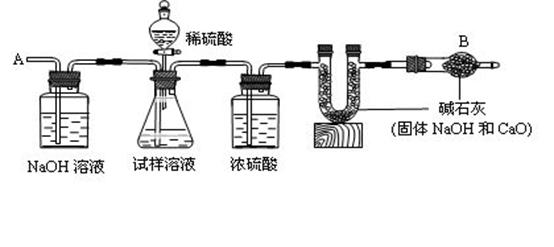
已知某纯碱试样中含有杂质氯化钠,为测定试样中纯碱的质量分数,可用下图装置进行实验。
 主要步骤如下,请填空:
主要步骤如下,请填空:
① 按图组装仪器,并检查装置的气密性② 将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;③ 称量盛有碱石灰的U形管的质量为b g;④ 从分液漏斗中滴入6mol/L的稀硫酸,直到不再产生气体为止,⑤ 从导管A处缓缓鼓入一定量的空气;⑥ 再次称量盛有碱石灰的U形管的质量为c g;⑦ 重复⑤和⑥的操作,直到U形管的质量基本不变,测得质量为d g。
回答下列问题:(碱石灰是一种干燥剂,不能干燥酸性气体)
(1)装置中干燥管B的作用是
(2)如果将分液漏斗中的硫酸换成同浓度的盐酸,测试的结果将 (填偏高.偏低或不变)
(3)步骤⑤的目的是
(4)步骤⑦的目的是
(5)该试样中纯碱的质量分数的计算式为
查看答案和解析>>
科目: 来源: 题型:
已知铜在常温下能被稀HNO3溶解,反应为:3Cu+8HNO3 3Cu(NO3)2+2NO↑+4H2O。
(1)请将上述反应改写成离子方程式_______。
(2)上述反应中,氧化剂是________(填化学式),氧化产物是_________(填化学式)。
(3)用双线桥法标出该反应的电子转移方向和数目。
(4)氧化剂与氧化产物的物质的量之比是________________
(5)此反应若生成NO 67.2L(标准状况),则转移了_______ mol 电子
查看答案和解析>>
科目: 来源: 题型:
将碱溶液A、盐溶液B按如下程序进行实验,根据下述现象判断:
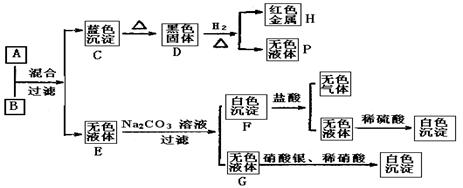
(1)A的化学式 B的化学式 。
(2)完成下列转化的化学方程式,并用“单线桥法”标明电子转移的方向和数目:
D+H2=H+P:
(3) 写出下列反应的离子方程式:
A+B:
F+盐酸:
(4)盐溶液B中阴离子的检验方法是
查看答案和解析>>
科目: 来源: 题型:
(1)1.5molH2SO4的质量是____________;
(2)9.03×1023个氨分子中的质子物质的量是_________;
(3)标况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为_______________;
(4)71.5g碳酸钠晶体(Na2CO3·10H2O)溶于水,配成500ml溶液,此溶液的物质的量浓度为______________。
查看答案和解析>>
科目: 来源: 题型:
已知NH4+ + OH- ![]() NH3↑ + H2O,NH3能使湿润的红色石蕊试纸变蓝。现某溶液中可能含有下列6种离子中的某几种:Na+、NH4+、K+、Cl-、SO42-、CO32-。为确认溶液组成进行如下实验:(1)取200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是( )
NH3↑ + H2O,NH3能使湿润的红色石蕊试纸变蓝。现某溶液中可能含有下列6种离子中的某几种:Na+、NH4+、K+、Cl-、SO42-、CO32-。为确认溶液组成进行如下实验:(1)取200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是( )
A、一定存在SO42-、CO32-、NH4+,可能存在Na+、K+、Cl-
B、一定存在SO42-、CO32-、NH4+、Cl-,一定不存在Na+、K+
C、c(CO32-)=0.01 mol/L,c(NH4+)>c(SO42-)
D、如果上述6种离子都存在,则c(Cl-)>c(SO42-)
查看答案和解析>>
科目: 来源: 题型:
某溶液中含有Cl-和I-的物质的量浓度相同。为了氧化I-而不使Cl-氧化,试根据下列三个反应判断,可选用的氧化剂是( )
①2Fe3++2I-=2Fe2++I2 ②2Fe2++Cl2=2Fe3++2I-
③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O
A.FeCl2 B.KMnO4 C.浓盐酸 D.FeCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com