
科目: 来源: 题型:
反应2SO2+O2![]() 2SO3 ,经一段时间后SO3的浓度增加了0.4mol·L-1 ,在这段时间内用O2表示的反应速率为0.4mol·L-1·s-1 ,则这段时间为 ( )
2SO3 ,经一段时间后SO3的浓度增加了0.4mol·L-1 ,在这段时间内用O2表示的反应速率为0.4mol·L-1·s-1 ,则这段时间为 ( )
A.0.1s B.2.5s C.0.5s D.10s
查看答案和解析>>
科目: 来源: 题型:
反应FeO(s)+C(s)=Fe(s)+CO(g); △H>0,ΔS>0,下列说法正确的是( )
A.低温下自发进行,高温下非自发进行 B 高温下自发进行,低温下非自发进行
C.任何温度下均为非自发进行 D任何温度下均为自发进行
查看答案和解析>>
科目: 来源: 题型:
在由水电离出的c(H+)= 1×10-13 mol·L-1的溶液中一定大量共存的离子组是( )
A. Fe2+, Na+, NO3-, Cl- B. Ba2+,Na+, NO3-,Cl-
C.SO42-,S2O32-,NH4+,Na+ D.Mg2+,Na+,Br -,AlO2-
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.强极性键形成的化合物不一定是强电解质
B.强电解质溶液的导电能力一定比弱电解质溶液强
C.NaCl溶液在电流的作用下电离成钠离子和氯离子
D.氯化钠晶体不导电是由于氯化钠晶体中不存在离子
查看答案和解析>>
科目: 来源: 题型:
下列关于平衡常数K的说法中,正确的是( )
A.在任何条件下,化学平衡常数是一个恒定值
B.改变反应物浓度或生成物浓度都会改变平衡常数K
C.平衡常数K只与温度有关,与反应浓度、压强无关
D.从平衡常数K的大小不能推断一个反应进行的程度
查看答案和解析>>
科目: 来源: 题型:
将10g氢气和40g氧气混合点燃,放出714.5KJ热量,同样条件下1mol氢气在氧气中完全燃烧放出的热量是( )
A.71.45KJ B.142.9KJ C.571.6KJ D.285.8KJ
查看答案和解析>>
科目: 来源: 题型:
把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为( )
A.1:2:3 B.3:2:1 C.6:3:1 D.6:3:2
查看答案和解析>>
科目: 来源: 题型:
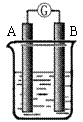
某研究性学习小组欲探究原电池的形成条件,按右图所示装置进行实验
| 序号 | A | B | 烧杯中的液体 | 指针是否偏转 |
| 1 | Zn | Cu | 稀硫酸 | 有 |
| 2 | Zn | Zn | 稀硫酸 | 无 |
| 3 | Cu | C | 氯化钠溶液 | 有 |
| 4 | Mg | Al | 氢氧化钠溶液 | 有 |
分析上述数据,回答下列问题:
(1)实验1中电流由 极流向 极(填“A”或“B”)
(2)实验4中电子由B极 流向A极 ,表明负极是 电极(填“镁”或“铝”)
(3)实验3 表明 A.铜在潮湿空气中不会被腐蚀 B.铜的腐蚀是自发进行的
(4)分析上表有关信息,下列说法不正确的是
A.相对活泼的金属一定做负极
B.失去电子的电极是负极
C.烧杯中的液体,必须是电解质溶液
D.浸入同一电解质溶液中的两个电极,是活泼性不同的二种金属(或其中一种非金属)
查看答案和解析>>
科目: 来源: 题型:
在常温下,下列五种溶液:①0.1mol/L NH4Cl ②0.1mol/L CH3COONH4
③ 0.1mol/L NH4HSO4 ④0.1mol/L NH3·H2O和0.1mol/L NH4Cl混合液 ⑤0.1mol/L NH3·H2O请根据要求填写下列空白:
(1)溶液①呈 性(填“酸”、“碱”或“中”),其原因是
(用离子方程式表示)
(2)在上述五种溶液中,pH最小的是 ;c(NH4+)最小的是 ﹝填序号﹞
(3)比较溶液②、③中c(NH4+)的大小关系是② ③ ﹝填“>”、“<”或“=”)
(4)在溶液④中, 离子的浓度为0.1mol/L;NH3·H2O和 离子的物质的量浓度之和为0.2 mol/L
(5)常温下,测得溶液②的pH=7,则说明CH3COO-的水解程度________(填“>”、“<”或“=”) NH4+ 的水解程度,CH3COO-与NH4+浓度的大小关系是:c(CH3COO-) c(NH4+)(填“>”、“<”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com