
科目: 来源: 题型:
火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2=Cu2S+2FeS+SO2,下列说法正确的是 ( )
A.SO2既是氧化产物又是还原产物
B.CuFeS2仅作还原剂,硫元素被氧化
C.每生成1molCu2S,有4mol硫被氧化
D.每转移1.2mol电子,有0.4mol硫被氧化
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是 ( )
A.用氨水吸收少量SO2气体:2NH3·H2O + SO2 = 2NH4+ +SO32—+ H2O
B.过氧化钠固体与水反应:2O22—+2H2O = 4 OH—+ O2↑
C.NH4HCO3溶液与过量的NaOH溶液反应:NH4+ +OH—= NH3↑+ H2O
D.Cl2通入水中:Cl2 + H2O = 2H+ + Cl—+ ClO—
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数,下列说法中,正确的是 ( )
A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA
B.常温常压下,18gH2O中含有的原子总数为3NA
C.标准状况下,11.2 L CH3CH2OH 中含有的分子数目为0.5NA
D.常温常压下,2.24 L CO 和CO2 混合气体中含有的碳原子数目为0.1NA
查看答案和解析>>
科目: 来源: 题型:
下列说法中不正确的是 ( )
A.Na2O2、HClO、SO2等物质都具有漂白作用。
B.在水溶液或熔融状态下能够导电的化合物中一定存在离子键
C.液态氯化氢、熔融氧化铝、固体硫酸钡都是电解质
D.非金属氧化物不一定是酸性氧化物,有些金属氧化物也能与强碱反应
查看答案和解析>>
科目: 来源: 题型:
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:

请回答下列问题:
(1)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为___ __(填代号),检验溶液A中Fe3+的最佳试剂为___ _(填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、_______ _、过滤等操作。
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)________(填化学式)。若实验过程中有氨气逸出,应选用下列_____ ___(填代号)装置回收。

写出制备碳酸钙的化学方程式
(4)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时视线应_____ __ _ ,直到_____ _ __。用KMnO4标准溶液滴定时应选用______ __滴定管((填“酸式”或“碱式”)。
(5)已知:无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
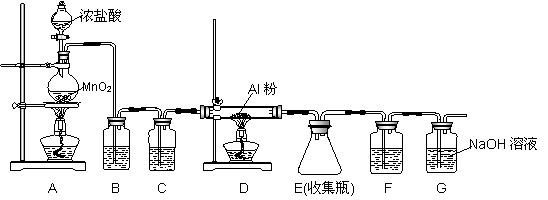

①写出A中反应的离子方程式
②装置B中盛放饱和NaCl溶液,该装置的主要作用是 。F中试剂的作用是 。用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为 _。
查看答案和解析>>
科目: 来源: 题型:
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:I:向废液中投入过量铁屑,充分反应后分离出固体和滤液:
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
己知:Ksp[Fe(OH)3]= 4.0×10-38 回答下列问题:
(1)FeCl3蚀刻铜箔反应的离子方程式为 :
(2)过程I 加入铁屑的主要作用是 ,分离得到固体的主要成分是 ,从固体中分离出铜需采用的方法是 ;
(3)过程II中发生反应的化学方程式为 ;
(4)过程II中调节溶液的pH为5,金属离子浓度为 。(列式计算)
查看答案和解析>>
科目: 来源: 题型:
已知A(g)+B(g) ![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| |温度/ ℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。,则6s时c(A)= mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为 ;
(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c. c(A)不随时问改变 d.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。
查看答案和解析>>
科目: 来源: 题型:
实验室需要0.1 mol·L-1 NaOH溶液460 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是____________(填序号),配制上述溶液还需用到的玻璃仪器是_______ __(填仪器名称)。

(2)下列操作中,容量瓶所不具备的功能有 。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.稀释液体溶质
E.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为 g。在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度 0.1 mol·L-1(填“大于”、“等于”或“小于”)。
(4)根据计算可知,需用量筒量取质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积
为 mL
查看答案和解析>>
科目: 来源: 题型:
下列溶液中微粒浓度关系一定正确的是
A.氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH![]() )
)
B.pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+)
C.0.1 mol·L-1的硫酸铵溶液中:c(NH![]() )>c(SO
)>c(SO![]() )>c(H+)
)>c(H+)
D.0.1 mol·L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目: 来源: 题型:
为探究锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是
A.加入NH4HSO4固体,v(H2)不变 B.加入少量水,v(H2)减小
C.加入CH3COONa固体,v(H2)减小 D.滴加少量CuSO4溶液,v(H2)减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com