
科目: 来源: 题型:阅读理解
平衡指的是两个相反方向的变化最后所处的运动状态;中学阶段涉及的平衡有气
体可逆反应的平衡、酸碱电离平衡、水解平衡及沉淀—溶解平衡等等。
(1)现有容积为2L的恒温恒容密闭容器,向其中加入2molA气体和2molB气体后发
生如下反应: A(g)十B(g)![]() C(g)
C(g) ![]()
20s后,反应达到平衡状态,生成lmolC气体,放出热量Q1kJ。回答下列问题。
①计算 20s内B气体的平均化学反应速率为 ,求出该反应的平衡常数
。
②保持容器温度和容积不变,若改为向其中加入1molC气体,反应达到平衡时,吸收热量QkJ,则Q1与Q2的相互关系正确的是 (填字母)。
(A)Ql+Q2=a (B)Q1+2Q2<2a (C) Q1+2Q2>2a (D) Ql+Q2<a
(2)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用合成气制备甲醇。反应为CO(g)+2H2(g)![]() CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关 其相关数据见下图:
CH3OH(g)某温度下,在容积为2L的密闭容器中进行该反应,其相关 其相关数据见下图:

①tmin至2tmin时速率变化的原因可能是 ;
②3tmin时对反应体系采取了一个措施,至4tmin时CO的物质的量为0.5mol,请完成上图CO的变化曲线。
(3)常温下,将VmL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mol·L-1醋酸
溶液中,充分反应。回答下列问题。(忽略溶液体积的变化)
①如果溶液pH=7,此时V的取值 20.00(填“>”、“<”或“="),而溶液中。c(Na+)、
以![]() 的大小关系;
的大小关系;
。
②如 果 V=40.00,则 此 时 溶液 中 ![]()
mol·L-1
(4)某温度条件下,若将CO2(g)和H2(g)以体积比1:4混合,在适当压强和催化剂
作用下可制得甲烷,己知:
![]()
则CO2(g)和H2(g)反应生成液态水的热化学方程式为:
查看答案和解析>>
科目: 来源: 题型:
铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如下图所示装置探究钢铁的腐蚀与防护。

在相同条件下,三组装置中铁电极腐蚀最快的是 (填装置序号),该装置中正极电极反应式为 ;为防止金属Fe被腐蚀,可以采用上述
(填装置序号)装置原理进行防护;装置③中总反应的离予方程式为
。
(2)新型固体LiFePO4隔膜电池广泛应用于电动汽车。
|
|
负极反应为Li-e-=Li+,则正极反应式为 。
(3)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:回答下列问题:
①操作I、Ⅱ的名称分别是 、 。
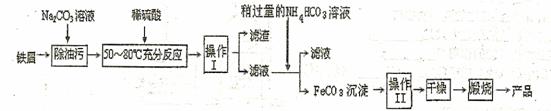
②写出在空气中锻烧FeCO3的化学方程式 ;
(4)有些同学认为![]() 溶液滴定也能进行铁元素含量的测定(
溶液滴定也能进行铁元素含量的测定(![]() )。
)。
a.称取2.850g绿矾 (FeSO4·7H2O)产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/KMnO4溶液滴定至终点,消耗![]() 溶液体积的平均值为 20.00mL。计算上述样品中FeSO4·7H2O的质量分数为
溶液体积的平均值为 20.00mL。计算上述样品中FeSO4·7H2O的质量分数为
查看答案和解析>>
科目: 来源: 题型:
CuSO4•5H2O是一种重要的化工原料。实验室以Cu为原料制取CuSO4·5H2O
![]() 有如下方法:
有如下方法:
方法一:
 (1)该方法中金属铜应在 (填仪器名称)中灼烧。
(1)该方法中金属铜应在 (填仪器名称)中灼烧。
方法二:
(2)该方法中少量![]() 起催化作用,其催化机理为(用离子方程式表示)
起催化作用,其催化机理为(用离子方程式表示)
![]() , 。调节溶液PH3~4,可使
, 。调节溶液PH3~4,可使![]() 完全转化为
完全转化为![]() 沉淀,调节时加入的试剂为 。
沉淀,调节时加入的试剂为 。
 方法三:
方法三:
(3)①该方法中首先要将Cu与稀硫酸和稀硝酸混合。为了只得到
 CuSO4溶液,需向100mLl.0moI• L-1稀硝酸中加入 mL 1.0mol·L-1稀硫酸与之混合。
CuSO4溶液,需向100mLl.0moI• L-1稀硝酸中加入 mL 1.0mol·L-1稀硫酸与之混合。
②Cu与稀硫酸和稀硝酸的反应装置如右图所示:
实验室中对圆底烧瓶加热的最佳方式是 ;
装置中圆底烧瓶上方长导管的作用是 。
③下列可做为右图中尾气收集或吸收装置的是 (填字母)。
(提示:![]()

(4)上述方法中,方法一耗能大,方法二步骤多,方法三生成有毒气体。请综合考虑有关
设 计 因 素 , 设 计 一 个 实 验 室 制 备 CuSO4·5H2O的 方 案 流 程
图 。
供选择的试剂:Cu、![]() 、
、![]() 、
、![]() 、浓硫酸、稀盐酸、稀硫酸等
、浓硫酸、稀盐酸、稀硫酸等
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物。
请回答下列问题:
(l)B的原子结构示意图 ;
(2)C、D、E三种原子对应的离子半径由大到小的顺序是 (填具体离子符号);由
A、B、C三种元素按 4:2:3组成的化合物所含的化学键类型属于 。 (3)用某种废弃的金属易拉罐与 A、C、D组成的化合物溶液反应,该反应的离子方程式
为: 。
(4)C和E两元素相比较,非金属性较强的是 (填“元素名称”),可以验证该
结论的是 (填“序号”)。
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素的单质在常温下的状态
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(5)A、C两元素的单质与熔融K2CO3,组成的燃料电池,其负极反应式
用该电池电解lLlmol/LNaCl溶液,当消耗标准状况下1.l2LA2时, NaCl溶液的
PH= (假设电解过程中溶液的体积不变)
查看答案和解析>>
科目: 来源: 题型:
如图所示,装置 (Ⅰ)是一种可充电电池的示意图,装置 (Ⅱ)为电解池的示意图;装置
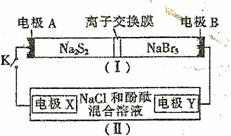 (Ⅰ)的离子交换膜只允许Na+通过。电池充、放电的化学方程式为:
(Ⅰ)的离子交换膜只允许Na+通过。电池充、放电的化学方程式为:
|
|
当闭合K时,X极附近溶液先变红色。下列说法中正确的是
A.装置(Ⅰ)中Na+从右到左通过离子交换膜
B.A电极的电极反应式为![]()
C.X电极的电极反应式为![]()
D.每有0.lmolNa+通过离子交换膜,x电极上就析出标准状况下的气体1.12L
查看答案和解析>>
科目: 来源: 题型:
取两个相同容积的密闭恒容容器,,在A容器中充入0.2molN2O4,B容器中充入0.2molHI
气体,在一定温度下反应分别达到平衡,测得N2O4和HI的分解率分别为![]() (A)和
(A)和![]() (B)。在该平衡体系中再分别充入0.2molN2O4和0.2molHI,当反应重新达到平衡时,测得N2O4和HI的分解率分别为
(B)。在该平衡体系中再分别充入0.2molN2O4和0.2molHI,当反应重新达到平衡时,测得N2O4和HI的分解率分别为![]() (A)和
(A)和![]() (B)。下列判断一定正确的是( )
(B)。下列判断一定正确的是( )
A. ![]() (A) >
(A) > ![]() (A)
(A) ![]() (B) <
(B) < ![]() (B) B.
(B) B. ![]() (A) >
(A) > ![]() (A)
(A) ![]() (B) =
(B) = ![]() (B)
(B)
C. ![]() (A) <
(A) <![]() (A)
(A) ![]() (B) =
(B) = ![]() (B) D.
(B) D. ![]() (A) =
(A) = ![]() (A)
(A) ![]() (B) >
(B) >![]() (B)
(B)
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是 ( )
A.醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b
B.在滴有酚酞溶液的氨水里,加入NH4C1至溶液恰好无色,则此时溶液的pH<7
C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合,
c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)
D. pH=5.6的CH3COOH与CH3COONa混合溶液中,c(CH3COO-)<c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com