
科目: 来源: 题型:
常温下,某溶液中由水电离产生的c(H+)、c(OH-)满足c(H+)·c(OH-)=10-26,则下列各组离子在该溶液中一定可以大量共存的是
A.K+、Na+、AlO2-、Cl- B.Na+、Cl-、SO42-、HCO3-
C.NH4+、Fe3+、NO3-、SO42- D.Ba2+、Na+、Cl-、NO3-
查看答案和解析>>
科目: 来源: 题型:
.已知反应A2(g)+2B2(g)![]() 2AB2(g)△H <0,下列说法正确的
2AB2(g)△H <0,下列说法正确的
A.升高温度,正向反应速率减小,逆向反应速率增大
B.升高温度有利于正、逆反应速率增大,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡逆向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
科目: 来源: 题型:
已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol·L-1的一元酸HA与bmol·L-1的一元碱BOH等体积混合,可判断溶液呈中性的依据是
A.混合溶液中,![]() B.混合溶液的PH = 7
B.混合溶液的PH = 7
C.a = b D.混合溶液中,c(B+)+c(H+)=c(A-) +c(OH-)
查看答案和解析>>
科目: 来源: 题型:
下列关于原电池的叙述正确的是
A.构成原电池的正极和负极必须是两种不同的金属
B.任何化学反应只要是自发进行的放热反应都可以被设计成原电池
C.在原电池中,电子流出的一极是负极,该电极被还原
D.原电池是化学能转变为电能的装置,为外界提供电能
查看答案和解析>>
科目: 来源: 题型:
下列事实不能用勒夏特列原理解释的是
A.将氯化铁溶液加热蒸干最终得不到氯化铁固体
B.钢铁在潮湿的空气中容易生锈
C.实验室可用排饱和食盐水的方法收集氯气
D.常温下,将1 mL pH=3的醋酸溶液加水稀释至l00 mL,测得其PH<5
查看答案和解析>>
科目: 来源: 题型:
对于A2 + 3B2![]() 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是
A.υ(B2) = 0.8mol·L-1·s-1 B.υv(A2) = 0.4mol·L-1·s-1
C.υ(C) = 0.6mol·L-1·s-1 D.υ(B2) = 42mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
下列表述中正确的是
A.放热反应在常温下均能自发进行
B.已知反应CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-802.3kJ/mol,说明甲烷的燃烧热为802.3kJ/mol
C.反应热的大小与反应物和生成物的键能无关
D.含1molNaOH的溶液分别和含0.5molH2SO4、1mol HNO3的溶液反应,放出的热量相等
查看答案和解析>>
科目: 来源: 题型:
已知A、B、C、![]() D、E、F六种元素的原子序数依次递增,都位于前四周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍。E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同。F处于周期表中第9列。
D、E、F六种元素的原子序数依次递增,都位于前四周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍。E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同。F处于周期表中第9列。
(1)B、C、D三种元素的氢化物的沸点高低顺序为 ,稳定性顺序为 。
(2)同时含有A、B、D三种元素的化合物M是此类物质中为数不多的气体,且分子中所有原子共平面,则M中σ键和π键个数比为 ,B原子的杂化类型为 ,M能和水以任意比混溶的原因是 。
(3)C的最高价含氧酸根的空间构型为 ,E的基态原子的价电子排布式为
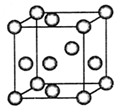
(4)“生物金属”E内部原子的堆积方式与铜相同,都是面心立方![]() 堆积方式,如图。则E晶胞中E的配位数为 ,若该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,E原子的摩尔质量为M g/mol,则E原子的半径为 cm
堆积方式,如图。则E晶胞中E的配位数为 ,若该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,E原子的摩尔质量为M g/mol,则E原子的半径为 cm
(5)F可形成分子式均为F(NH3)5BrSO4的两种配合物,其中一种化学式为[F(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,产生的现象是 ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com