
科目: 来源: 题型:
常温下,下列各组离子在制定溶液中一定能大量共存的是
A.0.1 mol·L-1的NaOH溶液:K+、Na+、SO42-、CO32-
B.0.1 mol·L-1的Na2CO3溶液:K+、Ba2+、NO3-、Cl-
C.0.1 mol·L-1FeCl3溶液:K+、NH4+、I-、SCN-
D.c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、NO3-
查看答案和解析>>
科目: 来源: 题型:
表示0.1mol·L-1NaHCO3溶液有关微粒浓度的关系正确的
A. c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-)
D.c(OH-)=c(H+)+c(H2CO3)+c(HCO3-)
查看答案和解析>>
科目: 来源: 题型:
下列说法中,正确的是
A.难溶电解质都是弱电解质
B.相同温度下,AgCl在水中的溶解能力与在NaCl溶液中的相同
C.难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解即停止
D.在白色ZnS沉淀上滴加CuSO4溶液,沉淀变黑色,说明CuS比ZnS更难溶于水
查看答案和解析>>
科目: 来源: 题型:
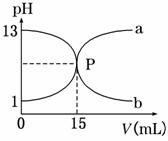
右图曲线a和b是盐酸与氢氧化钠的相互滴定的滴定曲线,下列叙述正确的是
A.盐酸的物质的量浓度为1 mol/L
B.酚酞不能作本实验的指示剂
C.曲线a是盐酸滴定氢氧化钠的滴定曲线
D.P点时反应恰好完全,溶液呈中性
查看答案和解析>>
科目: 来源: 题型:
下列有关的叙述,正确的是
A.Cl2的水溶液能导电,但Cl2是非电解质
B.0.1mol/L的醋酸钠溶液可以使酚酞试液变红,说明醋酸是弱电解质
C.纯碱溶解于水,水溶液温度升高,说明盐的水解是放热反应
D.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
查看答案和解析>>
科目: 来源: 题型:
室温下,在pH=1的硫酸溶液中,由水电离出来的H+浓度为
A. 0 B. 0.1 mol.L-1 C. 10-7 mol.L-1 D. 10-13 mol.L-1
查看答案和解析>>
科目: 来源: 题型:
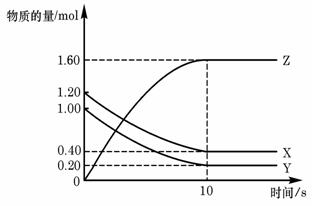
T ℃时,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是
A.平衡时X、Y的转化率相同
B.达到平衡后,将容器体积压缩为1 L,平衡向正反应方向移动
C.T ℃时,该反应的化学方程式为:X(g)+Y(g)![]() 2Z(g),平衡常数K= 40
2Z(g),平衡常数K= 40
D.向该密闭容器中充入少量稀有气体(不参加反应),平衡不移动
查看答案和解析>>
科目: 来源: 题型:
在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下它们反应生成NH3,10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
A.0.1mol.L-1.min-1 B.0.2mol.L-1.min-1
C.0.3mol.L-1.min-1 D.0.6mol.L-1.min-1
查看答案和解析>>
科目: 来源: 题型:
在一密闭容器中,反应mA(g)+nB(g)![]() pC(g),达到平时,测得c(A)为0.5 mol/L;在温度不变的条件下,将容器体积扩大一倍,当达到新平衡时,测得c(A)为0.3 mol/L。则下列判断正确的是
pC(g),达到平时,测得c(A)为0.5 mol/L;在温度不变的条件下,将容器体积扩大一倍,当达到新平衡时,测得c(A)为0.3 mol/L。则下列判断正确的是
A.化学计量数:m+n>p B.平衡向正反应方向移动
C.物质B的转化率增大 D.物质C的质量分数增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com