
科目: 来源: 题型:
下列实验操作能达到目的的是
A、用Na2S溶液和Al2(SO4)3溶液反应制取Al2S3固体
B、加热蒸发K2CO3溶液获得K2CO3晶体
C、加热蒸发FeCl2溶液制取Fe(OH)2固体
D、加热蒸发MgCl2溶液制取MgCl2固体
查看答案和解析>>
科目: 来源: 题型:
下列有关滴定操作的顺序正确的是
①检查滴定管是否漏水 ②用蒸馏水洗涤玻璃仪器
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管
④装标准溶液和待测液并调整液面(记录初读数)
⑤取一定体积的待测液于锥形瓶中 ⑥滴定操作
A、①③②④⑤⑥ B、①②③④⑤⑥ C、②③①④⑤⑥ D、④⑤①②③⑥
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A、pH=3和pH=4的盐酸各10mL混合,所得溶液的pH=3.5
B、溶液中c(H+)越大,pH值也越大,溶液的酸性就越强
C、液氯、液氨、液态氯化氢都不能导电,所以它们都不是电解质
D、当温度不变时,在纯水中加入强碱溶液不会影响水的离子积常数
查看答案和解析>>
科目: 来源: 题型:
H、C、N、O是几种重要的非金属元素。回答以下问题:
(1)C、N、O三种元素第一电离能从大到小的顺序是 。
(2)H3O+中H—O—H的键角比H2O中H—O—H的键角大,是因为 。
(3)与CO2是等电子体,可检验溶液中Fe3+的阴离子的电子式 。
(4)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮化物。
①肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)==3N2(g)+4H2O(g) △H=-1038.7 kJ/mol
若该反应中有4mol N—H键断裂,则形成的π键有___________mol。
②肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在________(填标号)
a、离子键 b、共价键 c、配位键 d、范德华力
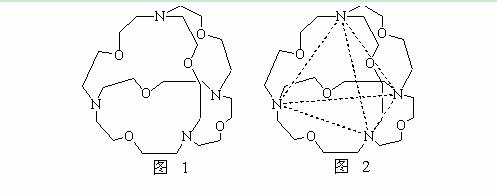
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是 (填标号)。
a、CF4 b、 CH4 c、 NH4+ d、H2O
查看答案和解析>>
科目: 来源: 题型:
有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。已知:A和C、B和D分别位于同主族,且B、D质子数之和是A、C质子数之和的2倍;E在同周期元素中原子半径最小。
(1)A2B和A2D的沸点较高者是________(填化学式),其原因是_______________________。
(2)与A3B+互为等电子体的分子为_________________。
(3)B形成的双原子分子里,从轨道重叠的角度来看共价键的类型有________。
(4)E原子的电子排布式为______________________。
查看答案和解析>>
科目: 来源: 题型:
有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E的顺序增大。C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2反应生成C2A与气态物质EB4;E的M层电子数是K层电子数的2倍。
(1)写出这五种元素的名称:A________,B________,C________,D________,E________。
(2) EB4的空间构型是 E原子是 杂化.
查看答案和解析>>
科目: 来源: 题型:
铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)写出基态铜原子的核外电子排布式 。
(2)SO42ˉ的立体构型是 ,其中S原子的杂化轨道类型是 。
查看答案和解析>>
科目: 来源: 题型:
氯原子的结构示意图为________,最外层电子对应的主量子数为________,角量子数取值可以为________,核外电子的运动状态共有________种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com