
科目: 来源: 题型:
已知5种短周期元素的原子序数大小关系为:C>A>B>D>E,A、C同周期,B、C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。
试回答下列问题:
(1)写出5种元素的名称:A________B________C________D_______E_______
(2)用电子式表示离子化合物A2B的形成过程:_____________________________
(3)按照要求回答:
D元素形成的单质的结构式是_______________;
D、E形成的共价化合物的电子式是___________;
B离子的结构示意图是_________________。
查看答案和解析>>
科目: 来源: 题型:
在一个小烧杯里,加入20gBa(OH)2·8H2O粉末,将小烧杯放在事先滴有4~5滴水的玻璃片上,然后加入10gNH4Cl晶体,并用玻璃棒迅速搅拌。回答下列问题:
(1)实验中玻璃棒的作用是___________________________________。
(2)反应的化学方程式:_______________________________________________。该反应属于_____________(填反应类型)。
(3)实验中观察到的现象有____________________________________________
通过_________现象,说明该反应为_______热反应,由此可推知反应物总能量__________(填大于,小于)生成物总能量。
查看答案和解析>>
科目: 来源: 题型:
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、__________、__________。
(2)量取反应物时,取50mL0.50mol·L-1的盐酸,还需加入的试剂是_____(填字母)
A.50mL0.50mol·L-1NaOH溶液
B.50mL0.55mol·L-1NaOH溶液
C.1.0gNaOH固体
(3)向1L 1mol·L-1NaOH溶液中分别加入稀醋酸、浓硫酸和稀硝酸,恰好反应时放热分别为Q1、Q2、Q3,则其由小到大的顺序为__________________________。
查看答案和解析>>
科目: 来源: 题型:
已知化学反应2C(s)+O2(g)=2CO(g),2CO(g)+O2(g)=2CO2(g)都是放热反应。据此判断,下列说法中不正确的是( )
A.12g C所具有的能量一定高于28gCO所具有的能量
B.56gCO和32gO2所具有的总能量大于88gCO2所具有的总能量
C.12gC和32gO2所具有的总能量大于44gCO2所具有的总能量
D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多
查看答案和解析>>
科目: 来源: 题型:
已知氢化锂(LiH)属于离子化合物,LiH跟水反应可以放出氢气。下列叙述中正确的是 ( )
A.LiH跟水反应后的溶液显中性
B.LiH在化学反应中是一种强氧化剂
C.LiH中氢离子可以被还原成氢气
D.LiH中氢离子半径比锂离子半径大
查看答案和解析>>
科目: 来源: 题型:
运用元素周期律分析下面推断,不正确的是 ( )
①H-的半径比Li+的半径大②砹(At)为有色固体,HAt不稳定③锂(Li)在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱④硫酸锶(SrSO4)是难溶于水的白色固体⑤硒化氢(H2Se)是无色、有毒、比H2S稳定的气体
A.①②④ B.③⑤ C. ②④⑤ D.③④
查看答案和解析>>
科目: 来源: 题型:
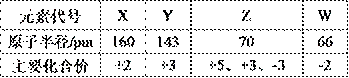
几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是 ( )A.X、Y元素的金属性X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.X和Y的最高价氧化物的水化物能够反应生成盐
查看答案和解析>>
科目: 来源: 题型:
下列关于元素金属性、非金属性的说法中,正确的是 ( )
A.F2和NaCl溶液的反应可证明氟的非金属性强于氯
B.H2SO3的酸性强于H2CO3,则非金属性:S > C
C.1mol金属A比1mol金属B在足量酸中置换出的H2多,说明A的金属性强于B
D.非金属性最强的元素是氟,表现在化合价上是氟无正价
查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y2-与Z+核外电子层的结构相同。下列化合物中同时存在极性和非极性共价键的是( )
A. Z2Y B. X2Y2 C. Z2Y2 D. ZYX
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com