
科目: 来源: 题型:
下列叙述正确的是
A.ⅠA族元素单质的熔点从上往下逐渐降低
B.分子晶体中一定存在共价键
C.ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
D.同周期非金属氧化物对应的水化物的酸性从左往右依次增强
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E是同周期的5种元素,A和B的最高价氧化物对应的水化物呈碱性,且碱性B>A;C和D的最高价氧化物对应的水化物呈酸性,且酸性C>D;5种元素所形成的简单离子中,E的离子半径最小,则它们的原子序数由大到小的顺序是ks5u
A.C、D、E、A、B B.E、C、D、A、B C.B、A、E、D、C D.B、A、D、C、E
查看答案和解析>>
科目: 来源: 题型:
下列与金属腐蚀有关的说法正确的是
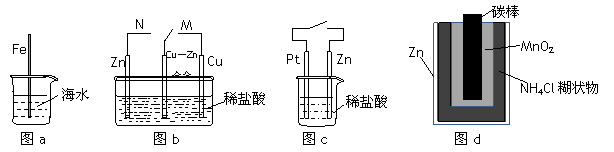
A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn - MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
查看答案和解析>>
科目: 来源: 题型:
①②③④ 四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②有气泡逸出;③④相连时,③的质量减少,据此判断这四种金属活动性由大到小的顺序是
A.①③②④ B.①③④② C.③④②① D.③①②④
查看答案和解析>>
科目: 来源: 题型:
20℃时,将10mL 0.1mol/L Na2S2O3溶液和10mL 0.1mol/L的H2SO4溶液混合,3min后溶液中明显出现浑浊。已知温度每升高10℃,化学反应速度增大到原来的3倍,那么40℃时,同样的反应要同样看到浑浊,需要的时间是
A.40s B.15s C.30s D.20s
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.常温常压下,1molC2H4所含的电子数为12 NA
B.标准状况下,16g甲烷中共价键数目为4NA
C.常温常压,4 g氦气所含的核外电子数为4NA
D.标准状况下,22.4L NO 与11.2L O2 充分反应后,所得的气体分子数一定为NA
查看答案和解析>>
科目: 来源: 题型:
下列有关化学用语使用正确的是ks5u
A. NH4Br的电子式:![]()
B. B.CO2的比例模型:![]()
![]()
|
D.中子数为20的氯原子: Cl
查看答案和解析>>
科目: 来源: 题型:
化学与社会、生活和生产息息相关,以下叙述错误的是
A.科学家们正在研究利用蓝绿藻等低等植物和微生物在阳光作用下使水分解产生氢气
B.贮氢金属在一定温度和压强下可以吸附氢气,如镧镍合金(LaNi5)可以吸附氢气形成LaNi5H6,其中H元素仍以H2分子形式存在
C.生活垃圾送入焚烧炉产生的热量可发电、供暖,焚烧炉产生的气体不可直接排放
D.2013年3月底,H7N9型禽流感在上海和安徽两地率先发现。要杀死禽流感病毒可通过消毒剂杀菌,通过加热煮沸杀菌,也可用紫外线照射杀菌。
查看答案和解析>>
科目: 来源: 题型:
已知T°C、pkPa时,在容积为vL的密闭容器内充有1molA和1molB。保持恒温、恒压反应A(g)+B(g) ![]() C(g)达到平衡时,C的体积分数为40%。试回答有关问题。
C(g)达到平衡时,C的体积分数为40%。试回答有关问题。
(1)欲使温度和压强在上述条件下恒定不变,在密闭容器内充入2molA 2molB,则反应达到平衡时,容器的容积为 ,C的体积分数为 。
(2)若另选一容积固定不变的密闭容器,仍控制温度为T℃,使1molA和1molB反应达到平衡状态时,C的体积分数仍为40%,则该密闭容器的容积为 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
某学习小组在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。为了进一步研究硫酸铜的量对氢气生成速率的影响,该小组同学开始了实验探究。
⑴实验方案:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的锥形瓶中,收集产生的气体。记录单位时间氢气产生的体积。
| 实验混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
其中:V1= ,V6= ,V9= ;
⑵实验装置:甲同学拟选用下列实验装置完成实验:

①你认为最简易的装置其连接顺序是:A接( )( )接( )( )接( )(填接口字母,可不填满。)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸就不能顺利滴入锥形瓶。请你帮助分析原因 。
③实验最后,在读取测量实验中生成氢气的总体积时,你认为合理的是 。
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
 ④ 乙同学认为可选用右图装置中的_____(填A或B)直接与锥形瓶的导管A相连用以测量氢气的体积,理由是 ;实验结束时量筒内的液面高于水槽中液面,立即读数会使氢气的总体积 (填“偏大”“偏小”或“不变”);应进行的操作是 ;
④ 乙同学认为可选用右图装置中的_____(填A或B)直接与锥形瓶的导管A相连用以测量氢气的体积,理由是 ;实验结束时量筒内的液面高于水槽中液面,立即读数会使氢气的总体积 (填“偏大”“偏小”或“不变”);应进行的操作是 ;
⑶实验现象与结论:反应一段时间后,实验A中的金属呈 色,实验E中的金属呈 色;该学习小组最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因 。
⑷问题讨论:实验室中现有![]() 、
、![]() 、
、![]() 、
、![]() 等4种溶液,可与实验中
等4种溶液,可与实验中![]() 溶液起相似作用的是 ;要加快上述实验中气体产生的速率,还可采取的措施有 (答两种);
溶液起相似作用的是 ;要加快上述实验中气体产生的速率,还可采取的措施有 (答两种);
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com