
科目: 来源: 题型:
向体积为Va的0.05 mol·L-1CH3COOH溶液中加入体积为Vb的0.05 mol·L-1KOH溶液,下列关系正确的是
A.Va=Vb时:c (CH3COO-)=c (K+)
B.Va=Vb时:c (CH3COOH) +c (H+)=c (OH-)
C.Va>Vb时:c (CH3COO-)>c (K+)> c (OH-)> c (H+)
D.Va与Vb任意比时:c (K+)+ c (H+) =c (OH-)+ c (CH3COO-)
查看答案和解析>>
科目: 来源: 题型:
已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是
A.该溶液的pH=4 B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目: 来源: 题型:
一定量的盐酸与过量的锌粉反应时,向盐酸中加入适量的下列物质,能减缓反应速率,但不影响生产H2的总量,适宜的方法组合为( )
①NaOH固体 ②H2O③NaCl溶液④CH3COONa溶液⑤NaNO3溶液
A、②③④⑤ B、②③④ C、全部 D、①②③④
查看答案和解析>>
科目: 来源: 题型:
从植物花汁中提取的一种有机物HIn,可做酸、碱指示剂,在水溶液中存在电离平衡:
HIn(红色)![]() H+ + In-(黄色)对上述平衡解释不正确的是
H+ + In-(黄色)对上述平衡解释不正确的是
A.升高温度平衡向正方向移动
B.加入盐酸后平衡向逆方向移动,溶液显红色
C.加入NaOH溶液后平衡向正方向移动,溶液显黄色
D.加入NaHSO4溶液后平衡向正方向移动,溶液显黄色
查看答案和解析>>
科目: 来源: 题型:
已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)的值增大,可以采取的措施是①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸 ④加水
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)的值增大,可以采取的措施是①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸 ④加水
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目: 来源: 题型:
右图所示为8000C时A、B、C三种气体在密闭容器中反应时浓度的变化只从图上分析不能得出的结论是
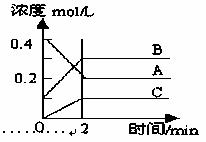
A.A是反应物
B.前2 min A的分解速率为0.1mol•L-1•min-1
C.达平衡后,若升高温度,平衡向正反应方向移动
D.达平衡后,若增大压强,平衡向逆反应方向移动
查看答案和解析>>
科目: 来源: 题型:
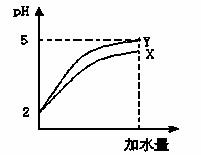
常温下pH均为2的两种酸溶液X和Y各10 mL分别加水稀释到10000 mL,其pH与所加水的体积变化如图所示,下列结论中正确的是
A.加水后,Y酸的电离度增大
B.X酸在水溶液中存在电离平衡
C.加水后,X酸的电离平衡常数减小
D.X酸的物质的量浓度与Y酸的物质的量浓度相等
查看答案和解析>>
科目: 来源: 题型:
列各电离方程式中,书写正确的是
A.CH3COOH ![]()
![]() H++CH3COO- B.KHSO4
H++CH3COO- B.KHSO4 ![]()
![]() K++H++SO
K++H++SO![]()
C.Al(OH)3===Al3++3OH- D.NaH2PO4 ![]()
![]() Na++H2PO
Na++H2PO![]()
查看答案和解析>>
科目: 来源: 题型:
关于小苏打水溶液的表述正确的是
A. c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B. HCO3-的电离程度大于HCO3-的水解程度
C. c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
D. 存在的电离只有:NaHCO3=Na+ + HCO3- ,
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是
A.反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H<0
B.常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小
C.在溶液中导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质
D.温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com