
科目: 来源: 题型:
在水中加入等物质的量的Ag+、Pb2+、Na+、SO42-、 NO3-、Cl-,该溶液放在用惰性材料做电极的电解槽中,通电片刻,则氧化产物和还原产物的质量之比
A.35.5:108 B.16:207 C.8:1 D.108:35.5
查看答案和解析>>
科目: 来源: 题型:
实验室制乙酸乙酯1 mL后,沿器壁加入紫色石蕊试液0.5 mL,这时石蕊试液将存在于饱和碳酸钠溶液层与乙酸乙酯层之间(整个过程不振荡)。对可能出现的现象,下列叙述中正确的是( )
A.石蕊层仍为紫色,有机层无色
B.石蕊层为三层环,由上而下是红、紫、红
C.石蕊层有两层,上层为紫色,下层为蓝色
D.石蕊层为三层环,由上而下是蓝、紫、红
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.石油的分馏和煤的干馏均为化学变化
B.2,3一二甲基丁烷的核磁共振氢谱中会出现两个峰
C.汽油和植物油的主要成分都是碳氢化合物
D.纤维素和淀粉遇碘水均显蓝色
查看答案和解析>>
科目: 来源: 题型:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)
2NO2(g)体系中,n(NO)
随时间的变化如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010. | 0.008 | 0.007 | 0.007 | 0.007 |
⑴写出该反应的平衡常数表达式:K= 。
 已知:
已知:![]() >
>![]() ,则该反应是 热反应。
,则该反应是 热反应。
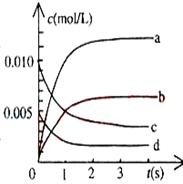
⑵右图中表示NO2的变化的曲线是 。
用O2表示从0~2s内该反应的平均速率v= 。
⑶能说明该反应已达到平衡状态的是 。
a.v (NO2)=2 v (O2) b.容器内压强保持不变
c.v逆 (NO)=2 v正 (O2) d.容器内密度保持不变
⑷ 为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离出NO2气体 b.适当升高温度
![]() c.增大O2的浓度 d.选择高效催化剂
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目: 来源: 题型:
高炉炼铁过程中发生的主要反应为
![]()
 |
已知该反应在不同温度下的平衡常数如上:请回答下列问题:
(1)该反应的平衡常数表达式K= ,△H________0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min后达到平衡。求该时间范围内反应的平均反应速率υ(C02)= _____________、CO的平衡转化率= _____________:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是_____________。
A.减少Fe的量 B.增加Fe203的量 C.移出部分C02
D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂
查看答案和解析>>
科目: 来源: 题型:
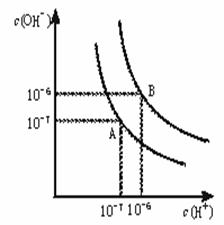
水的电离平衡曲线如右图所示。
(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 。
(2)将100℃时的pH=8的氢氧化钠溶液与100℃时的pH=5的稀硫酸混合(体积变化忽略不计),并保持100℃的恒温,欲使混合溶液pH=7,则氢氧化钠与硫酸的体积比为 。
查看答案和解析>>
科目: 来源: 题型:
为比较Fe3+和Cu2+对H2O2分解的催化效果,甲、乙同学分别设计了如图一、图二所示的实验。
(1) H2O2分解的化学方程式为 。
 |
图一 图二
(2)图一所示实验能定性说明反应快慢的依据是 _______________________________;
图二所示实验能说明反应快慢的数据是____________________________________。
(3)① 用H2O2和H2SO4的混合溶液可溶解印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H= + 64.39 kJ/mol
2H2O2(l)=2H2O(l) + O2(g) △H= ﹣196. 46 kJ/mol
H2(g) + 1/2O2(g) = H2O(l) △H= ﹣285. 84 kJ/mol
在H2SO4溶液中Cu与H2O2反应生成Cu2+ 和H2O的热化学方程式为:
。
② 控制其他条件相同,印刷电路板的金属粉末用10% H2O2和3 .0 mol/L H2SO4的混
合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
铜平均溶解速率 (×10—3 mol·L-1·min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因
是 。
查看答案和解析>>
科目: 来源: 题型:
用已知浓度的盐酸溶液滴定未知浓度的烧碱溶液,下列错误操作将对c(碱)
有何影响?(填写:偏大、偏小或无影响)
A、盛标准酸的滴定管尖嘴部分有气泡未排除就开始滴定( )
B、振荡时液体飞溅出来 ( )
C、开始读标准酸时用仰视 ( )
D、终点读标准酸时用俯视 ( )
E、滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥( )
查看答案和解析>>
科目: 来源: 题型:
根据所给信息写出下列化学反应的热化学方程式:
(1)C和1 mol水蒸气生成H2和CO时吸收131.5 kJ。
。
(2)甲硅烷(![]() )是一种无色气体,遇到空气能发生爆炸性自燃,生成
)是一种无色气体,遇到空气能发生爆炸性自燃,生成![]() 和水。
和水。
已知室温下1g甲硅烷自燃放出热量44.6 KJ,其热化学方程式是:
(3)已知:![]() △H=-393.5 KJ/mol
△H=-393.5 KJ/mol
![]() △H=-283.04 KJ/mol
△H=-283.04 KJ/mol
写出石墨燃烧生成CO的热化学方程式: 。
查看答案和解析>>
科目: 来源: 题型:
(1)实验室常用排饱和食盐水的方法来收集氯气,原因是:
(用离子方程式和简要的文字说明)
(2)在醋酸钠溶液中滴入酚酞,溶液呈 色,原因是
(用离子方程式表示),加热后颜色变 ,原因是 。
(3)盐碱地(含较多Na2CO3)不利于农作物生长,通过施加适量石膏(CaSO4•2H2O)
可以降低土壤的碱性。试用离子方程式分别表示盐碱地产生碱性的原因:
;用石膏可以降低其碱性的反应
原理: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com