
科目: 来源: 题型:
分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题。
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、 、 。
(2)为什么中和热测定中要用稍过量的碱(或酸):
(3) 假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g·℃)。为了计算中和热,某学生实验记录数据如下:
| 实验序号 | 起始温度t1℃ | 最高温度t2℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.1 | 20.1 | 23.2 |
| 2 | 20.2 | 20.2 | 23.1 |
| 3 | 20.5 | 20.5 | 25.3 |
依据该学生的实验数据计算,该实验测得的中和热△H=______;(结果保留一位小数)
(4)上述实验数值结果与中和热的理论值57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差 b.量取盐酸与氢氧化钠溶液时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度
查看答案和解析>>
科目: 来源: 题型:
现有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A、D同主族,C、E同主族,A、B的最外层电子数之和与C的最外层电子数相等, A能分别与B、C形成电子总数相等的分子M、N,且N为比较常见的液态化合物。请回答下列问题:
(1)B的简单阴离子的结构示意图 。
(2)A、D、E三种元素组成的化合物电子式为: 。
(3)① C、D、E对应的简单离子的半径由大到小为 (用离子符号表示);
②写出能证明C和E非金属性强弱的一个化学方程式 。
(4)A、C、E三种元素能形成多种18电子分子,写出其中两种所能发生的反应方程式 。
(5)标况下,1gD单质在C单质中完全燃烧可放出QKJ热量。则此反应的热化学方程式为
。
查看答案和解析>>
科目: 来源: 题型:
在一定温度下,将等量的气体分别通入起始体积均为2L的密闭容器Ⅰ(保持温度、体积不变)和Ⅱ(保持温度、压强不变)中,使其发生反应,6min时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )
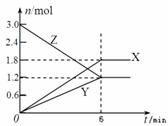
 |
A.该反应的化学方程式为:3Z = 3X+2Y
B.若两容器中均达到平衡时,则容器Ⅱ达到平衡所需时间大于t0
C.容器Ⅰ中,第5min时Z的消耗速率大于X的消耗速率
D.容器Ⅰ中,前6min内Z的反应速率为0.3mol/(L·min)
查看答案和解析>>
科目: 来源: 题型:
可以证明可逆反应N2 + 3H2![]() 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
①一个N≡N断裂的同时,有3个H-H键断裂 ②一个N≡N键断裂的同时,有6个N-H键断裂③其它条件不变时,混合气体平均式量不再改变④保持其它条件不变时,体系压强不再改变⑤NH3%、N2%、H2%都不再改变 ⑥恒温恒容时,密度保持不变
⑦正反应速率v(H2)=0.6mol/(L·min),逆反应速率v(NH3)=0.4mol/(L·min)
A.全部 B.只有①③④⑤ C.②③④⑤⑦ D.只有①③⑤⑥⑦
查看答案和解析>>
科目: 来源: 题型:
反应速率v和反应物浓度的关系是用实验方法测定的。化学反应H2+Cl2=2HCl的反应速率v可表示为v = k[c(H2)]m[c(Cl2)]n,式中k为常数,m、n值可用下表中数据确定之。
| c (H2)(mol/L) | c (Cl2) (mol/L) | v [mol/(L·s)] |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 4.0k |
由此可推得,m、n值正确的是 ( )
A. m=1、n=![]() B.m=
B.m=![]() 、n=
、n=![]() C.m=
C.m=![]() 、n=1 D. m=1、n=1
、n=1 D. m=1、n=1
查看答案和解析>>
科目: 来源: 题型:
反应3Fe(S)+ 4H2O(g)= Fe3O4(s)+ 4H2(g),在一可变的容积的密闭容器中进行,下列说法正确的是( )
A.增加Fe的量,其正反应速率增大
B.将容器的体积缩小一半,其正反应速率增大,逆反应速率减小。
C.保持体积不变,充入水蒸气使体系压强增大,其正反应速率增大,逆反应速率减小。
D.保持压强不变,充入N2使容器的体积增大,其正反应速率减小,逆反应速率也减小。
查看答案和解析>>
科目: 来源: 题型:
将2.24L甲烷(标况)和一定量氧气混合燃烧,得产物CO、CO2和水蒸气共7.2g ,当其缓慢经过无水CaCl2时,CaCl2增重3.6g,原混合气体中CO2的质量为( )
A.2.31 g B.4.4g C.3.3g D.2.2g
查看答案和解析>>
科目: 来源: 题型:
LiAl/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为: 2Li++FeS+2e-===Li2S+Fe,有关该电池的下列说法中,正确的是 ( )
A.LiAl在电池中作为负极材料,该材料中Li的化合价为+1价
B.该电池的电池反应式为:2Li+FeS===Li2S+Fe
C.负极的电极反应式为:Al-3e-===Al3+
D.放电时,电池中Li+移向负极
查看答案和解析>>
科目: 来源: 题型:
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内的离子“流过”水和氧化锌组成的电解液。电池总反应为: Zn + 2 MnO2十H2O == ZnO + 2MnO (OH)。下列说法正确的是( )
A.该电池的正极为锌
B.该电池反应中二氧化锰起催化剂作用
C.当 0.l mol Zn 完全溶解时,流经电解液的电子个数为 1.204×l023
D.电池正极反应式为: 2MnO2 + 2e -+2H2O ==2MnO (OH)+2OH-
查看答案和解析>>
科目: 来源: 题型:
有36g1H35Cl和80g3H37Cl,下列说法正确的是( )
A.两者所含中子数之比为1:2
B.分别与足量Na反应时,两者生成气体的质量之比为1:6
C.与NaOH溶液发生中和反应所消耗的NaOH的物质的量之比为1:1
D.两者所含质子数之比为9:22
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com