
科目: 来源: 题型:
下列各组元素的性质递变情况错误的是( )
A.Li、Be、B原子最外层电子数依次增多
B.P、S、Cl元素最高正价依次升高
C.N、O、F原子半径依次增大
D.Na、K、Rb的金属性依次增强
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.原子最外层电子数等于或大于3(小于8)的元素一定是非金属元素
B.原子最外层只有1个电子的元素一定是金属元素
C.最外层电子数比次外层电子数多的元素一定位于第二周期
D.某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第三周期
查看答案和解析>>
科目: 来源: 题型:
某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是( )
A.它是副族元素
B.它是第六周期元素
C.它的原子核内有63个质子
D.它的一种同位素的核内有89个中子
查看答案和解析>>
科目: 来源: 题型:
(8分)在101 KPa、150 ℃条件下,0.01 mol某烷烃充分燃烧后,将生成的气体通过盛有足量浓硫酸的洗气瓶,浓硫酸质量增重1.26 g ,然后再通过碱石灰,气体被完全吸收,碱石灰质量增加2.64 g。请回答下列问题:
(1)写出该烷烃的分子式: ,该烷烃有 种同分异构体;
(2)若该烷烃的一氯代物有两种同分异构体,写出该烷烃的结构简式并命名:
, 。
查看答案和解析>>
科目: 来源: 题型:
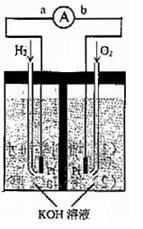
(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
(1)氢氧燃料电池的能量转化主要形式是 ,
在导线中电子流动方向为 (用a、b表示)。
(2)负极反应式为 。
(3)电极表面镀铂粉的原因为 。
(4)该电池工作时,H2和O2连续由外部供给,电池可连
续不断提供电能。因此,大量安全储氢是关键技术
之一。金属锂是一种重要的储氢材料,吸氢和放氢
原理如下:
Ⅰ.2Li + H2![]()
![]() 2LiH
2LiH
Ⅱ.LiH + H2O = LiOH + H2↑
① 反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
② 已知锂吸收224 L(标准状况)H2,生成的LiH与H2O完全反应,放出的H2用
作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
查看答案和解析>>
科目: 来源: 题型:
(8分)在1×105 Pa和298 K时,将1 mol气态AB分子分离成气态A原子和B原子所需要的能量称为键能(kJ·mol-1)。下面是一些共价键的键能:
| 共价键 | H-H | N≡N | N-H |
| 键能(kJ·mol-1) | 436 | 945 | 391 |
(1)上表中的数据判断工业合成氨的反应是______(填“吸热”或“放热”)反应;
(2)298 K时,取1mol N2和3mol H2放入一密闭容器中,在催化剂存在下进行反应。
若1 mol N2和3 mol H2完全反应放出或吸收的热量为Q1,则Q1为__________;
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是____________;
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2
如此选择的理由:___________________________________________。
查看答案和解析>>
科目: 来源: 题型:
 (10分)某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500 mL 0.5 mol·L-1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图。
(10分)某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500 mL 0.5 mol·L-1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图。
(1)关于图像的描述不正确的是 (填序号,下同);
① a → b段产生H2加快可能是表面的氧化膜逐渐溶解,加快了反应速率
② b → c段产生H2较快可能是该反应放热,导致温度升高,加快了反应
③ c以后,产生H2速率逐渐下降可能是铝片趋于消耗完全
(2)其他条件不变,现换用500 mL 1 mol·L-1盐酸,产生氢气速率普遍较使用500 mL
0.5 mol·L-1硫酸的快,可能的原因是________;
①盐酸中c(H+)的浓度更大 ②Cl-有催化作用 ③SO42-有催化作用 ④SO42-有阻化作用(使反应变慢) ⑤Al3+有催化作用
(3)要加快铝与硫酸溶液制H2的反应速率,小组成员提出一系列方案,比如:
①加入某种催化剂; ②加入蒸馏水; ③将铝片换成铝粉;
④增加硫酸的浓度至18 mol/L; ⑤ ; ⑥ _。
以上方案不合理的有 ;请你再补充两种合理方案,填入空白⑤⑥处。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E短周期元素,周期表中A与B,B与C相邻,A与C的最外层电子数之比为2:3,B的最外层电子数比E的最外层电子数少一个;常见化合物D2C2与水反应生成C的单质,且溶液可使酚酞试液变红。
(1)E的元素符号是 ;写出B在周期表中的位置 。
(2)A的氢化物的空间构型为 ;AC2的电子式为 ;A、B、C的氢化物稳定性顺序为 (用分子式表示)。
(3)B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z中化学键的类型有 。
(4)若A的氢化物中混有EC2杂质,可将混合气体依次通入 、
(用化学式填空),写出第一步的离子方程式 。
查看答案和解析>>
科目: 来源: 题型:
根据下列各组物质,回答问题(均填选项号):
A.O2与O3 B. 12C与13C C.正丁烷和异丁烷
D.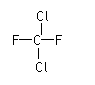 和
和 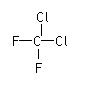 E.甲烷和庚烷 F.D与T
E.甲烷和庚烷 F.D与T G.金刚石与“足球烯”C60 H.16O、17O和18O
(1)互为同位素的是 ; (2)互为同素异形体的是 ;
(3)属于同系物的是 ; (4)互为同分异构体的是 ;
(5)属于同一物质的是 。
查看答案和解析>>
科目: 来源: 题型:
3 mol A和2.5 mol B混合于2 L密闭容器中,发生的反应如下:
3A(g)+B(g) ![]() xC(g)+2D(g)
xC(g)+2D(g)
5 min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.1 mol/(L·min),
下列结论正确的是( )
A.A的平均反应速率为 0.1 mol/(L·min)
B.平衡时,C的浓度为 0.125 mol/L
C.平衡时,B的转化率为 20%
D.平衡时,容器内压强为原来的 0.8 倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com