
科目: 来源: 题型:
下列电离方程式书写不正确的是( )
A.2H2O ![]() H3O++OH- B.H2S
H3O++OH- B.H2S ![]() H++HS-
H++HS-
C.NaHS ![]() Na++HS- D.HCO3—+H2O
Na++HS- D.HCO3—+H2O ![]() H3O++CO32-
H3O++CO32-
查看答案和解析>>
科目: 来源: 题型:
化学在工业生产和日常生活中有重要的应用。下列有关说法正确的是( )
A. CO2、NO2和SO2都是酸性氧化物,都是大气污染物
B. Na2O2、H2O2所含化学键完全相同,都能作供氧剂
C. 常温下,浓硫酸、浓硝酸与铁均能发生钝化且均能用铁罐储运
D. NaClO和明矾都能作消毒剂或净水剂,加入酚酞试液均显红色
查看答案和解析>>
科目: 来源: 题型:
下列有关物质分类或归类正确的是( )
①混合物:石炭酸、福尔马林、水玻璃、水银②化合物:CaCl2、烧碱、聚苯乙烯、HDO
③电解质:明矾、胆矾、冰醋酸、硫酸钡④同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
⑤同素异形体:C60、C70、金刚石、石墨
A.①③ B.③⑤ C.②③ D.②④
查看答案和解析>>
科目: 来源: 题型:
在537℃、1.01×105 Pa时,往容积可变的密闭容器中充入1 mol X和3 mol Y,此时容积为V L。保持恒温恒压,发生反应X(g)+3Y(g)![]() 2Z(g),达到平衡时,平衡混合气体中Z的体积分数为0.5。
2Z(g),达到平衡时,平衡混合气体中Z的体积分数为0.5。
(1) 达到平衡时,X的转化率约为 ▲ 。
(2) 保持上述温度和压强恒定不变,若向容器中只充入4 mol Z,则反应达到平衡时,平衡气体中Y 的体积分数为 ▲ ,容器的容积为 ▲ L。
(3) 若另选一容积固定不变的密闭容器,仍控制温度不变,使2 mol X和6 mol Y反应,达到平衡时平衡气体中Z的体积分数仍为0.5,则该密闭容器的容积为 ▲ 。
(4) 若温度仍为537℃,容器体积保持VL不变(恒容),往其中充入a mol X的b mol Y,使反应达到平衡,这时平衡气体中Z的体积分数仍为0.5,体系压强为1.01×105 Pa,若a: b = 1: 3,则a = ▲ 。
查看答案和解析>>
科目: 来源: 题型:
氨在国民经济中占有重要的地位,请参与下列探究。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。
C(s) + H2O(g) ![]() H2(g) + CO(g) △H = +131.3 kJ/mol,△S = +133.7 J/K
H2(g) + CO(g) △H = +131.3 kJ/mol,△S = +133.7 J/K
该反应在低温下能否自发 ▲ (填:能或否)。
(2)已知在400℃时,N2 (g)+ 3H2(g) ![]() 2NH3(g) △H<0 的K=0.5,
2NH3(g) △H<0 的K=0.5,
①2NH3(g)![]() N2 (g)+ 3H2(g)的K= ▲ (填数值)。
N2 (g)+ 3H2(g)的K= ▲ (填数值)。
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应V(N2)正 ▲ V(N2)逆(填:>、<、=、不能确定)
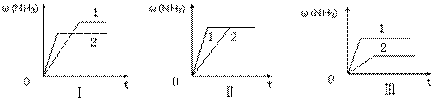
(3)在三个相同容器中各充入1 molN2和3molH2,在某一不同条件下反应并达到平衡,氨的体积分数随时间变化曲线如下图。下列说法正确的是 ▲ (填序号) 。
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ可能是同温同压下,催化剂性能,1>2
查看答案和解析>>
科目: 来源: 题型:
钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域.
(1)V2O5是接触法制硫酸的催化剂.
①一定条件下,![]() 与空气反映t min后,
与空气反映t min后,![]() 和
和![]() 物质的量浓度分别为a mol/L和b mol/L, 则
物质的量浓度分别为a mol/L和b mol/L, 则![]() 起始物质的量浓度为 ▲ mol/L ;生成
起始物质的量浓度为 ▲ mol/L ;生成![]() 的化学反应速率为
的化学反应速率为
▲ mol/(L·min) .
②工业制硫酸,尾气![]() 用____▲___吸收.
用____▲___吸收.
(2)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示.
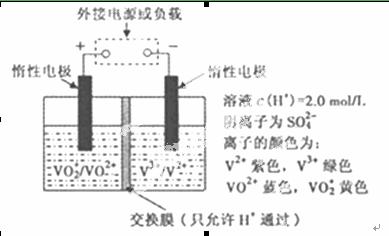
①当左槽溶液逐渐由黄变蓝,其电极反应式为 ▲ .
②充电过程中,右槽溶液颜色逐渐由 ▲ 色变为 ▲ 色.
③放电过程中氢离子的作用是 ▲ 和 ▲ ;充电时若转移的电子数为3.01![]() 1023个,左槽溶液中n(H+)的变化量为 ▲ .
1023个,左槽溶液中n(H+)的变化量为 ▲ .
查看答案和解析>>
科目: 来源: 题型:
在容积为2.0 L的密闭容器内,物质D在T ℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,据图回答下列问题:
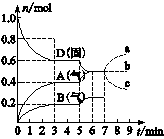
(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为_______ ▲ ___。
(2)根据图写出该反应的化学方程式___________________▲_________________________,
该反应的平衡常数表达式为K=______▲______。
(3)第5分钟时,升高温度,A、B、D的物质的量变化如图,则该反应是___▲_____(填“放热”或“吸热”)反应,反应的平衡常数_____▲___(填“增大”、“减小”或“不变”。下同),B的反应速率______▲____。
若在第7分钟时增加D的物质的量,A的物质的量变化正确的是____▲____(用图中a~c的编号回答)。
(4)某同学在学习了“化学反应速率和化学平衡”专题后,发表如下观点,你认为错误的是____▲____。
a.化学反应速率理论研究怎样在一定时间内快出产品
b.化学反应速率理论是研究怎样提高原料转化率
c.化学平衡理论是研究怎样使用有限原料多出产品
d.正确利用化学反应速率和化学平衡理论都可以提高化工生产的综合效益
查看答案和解析>>
科目: 来源: 题型:
可逆反应①X(g)+2Y(g)![]()
![]() 2Z(g) 、②2M(g)
2Z(g) 、②2M(g)![]() N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示: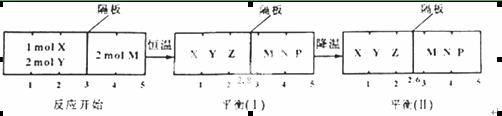
下列判断正确的是
A.反应①的正反应是吸热反应
B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C.达平衡(I)时,X的转化率为![]()
D.在平衡(I)和平衡(II)中M的体积分数相等
查看答案和解析>>
科目: 来源: 题型:
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) ![]()
![]() 2NH3(g) ΔH=-92.6 kJ/mol。实验测得起始、平衡时的有关数据如下表所示:
2NH3(g) ΔH=-92.6 kJ/mol。实验测得起始、平衡时的有关数据如下表所示:
| 容器编号 | 起始时各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15 kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述错误的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为![]()
C.容器②中达平衡时放出的热量Q=23.15 kJ
D.若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
查看答案和解析>>
科目: 来源: 题型:
T ℃时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图 (1)所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积分数与时间的关系如图 (2)所示。则下列结论正确的是
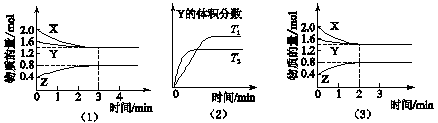
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
B.容器中发生的反应可表示为:3X(g)+Y(g)![]()
![]() 2Z(g)
2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图 (3)所示,则改变的条件是增大压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com