
科目: 来源: 题型:
下列离子方程式书写正确的是( )
A.向次氯酸钠溶液中通入少量二氧化硫:2ClO-+ SO2 + H2O = SO32- + 2HClO
B.用食醋除去水瓶中的水垢:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O
C.碳酸氢铵溶液与少量氢氧化钠溶液反应 ![]() + OH-
+ OH-![]() NH3·H2O
NH3·H2O
D.向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
查看答案和解析>>
科目: 来源: 题型:
关于氢键,下列说法不正确的是( )
A.每一个水分子内含有两个氢键
B.水的沸点很高原因之一是水分子间存在氢键
C.水非常稳定与水分子之间形成氢键无关
D.冰、水中都存在氢键
查看答案和解析>>
科目: 来源: 题型:
下列关于元素性质的有关叙述中正确的是( )
A.可以用HClO和H2SO3酸性的相对强弱来比较Cl和S的非金属性强弱
B.金属和非金属之间一定能形成离子化合物
C.碱金属元素单质,由Li→Fr,熔点逐渐降低
D.沸点:HI>HBr>HCl>HF
查看答案和解析>>
科目: 来源: 题型:
对相同状况下的12C18O和14N2两种气体,下列说法正确的是( )
A. 若质量相等,则质子数相等 B. 若原子数相等,则中子数相等
C. 若分子数相等,则体积相等 D. 若体积相等,则密度相等
查看答案和解析>>
科目: 来源: 题型:
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是( )
①在标准状况下,每消耗5.6L CH4可以向外电路提供2mole-
②通过甲烷电极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
③通过甲烷的电极为电池的正极,通过氧气的电极为负极
④电池放电后,溶液pH不断升高
A.①② B.①③ C.①④ D.③④
查看答案和解析>>
科目: 来源: 题型:
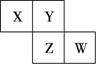
X、Y、Z、W均为短周期元素,在周期表中位置如图所示。Y原子的最外层电子数是电子层数的3倍。下列说法中不正确的是( )
A.Y、Z的气态氢化物,前者更稳定
B.Z、W的最高价氧化物对应水化物的酸性,前者强
C.X、W的气态氢化物相互反应,生成物中既含离子键又含共价键
D.Y、W的单质,均可通过电解的方法获得
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.当?H﹤0时,表示该反应为吸热反应
B.相同条件下,溶液中![]() 、
、![]() 、
、![]() 的氧化性依次减弱
的氧化性依次减弱
C.铅蓄电池在放电过程中,负极质量减小,正极质量增加
D.钢铁吸氧腐蚀的正极电极反应:O2+2H2O+4e-==4OH-
查看答案和解析>>
科目: 来源: 题型:
铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只生成4480mL的NO2气体和336mL的N2O4气体(标况下),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为( )
A.9.02g B.8.51g C.8.26g D.7.04g
查看答案和解析>>
科目: 来源: 题型:
已知Na2SO4 和NaCl混合溶液中,Cl-的物质的量浓度是Na+的物质的量浓度的![]() 倍,下列叙述中正确的是( )
倍,下列叙述中正确的是( )
A.Na2SO4 和NaCl的物质的量之比为1 :3
B.溶液中一定有1molNa2SO4和3molNaCl
C.所带电荷数SO42-是Na+的![]() 倍
倍
D. SO42- 与Cl-的物质的量之和等于Na+的物质的量
查看答案和解析>>
科目: 来源: 题型:
有Na2CO3、AgNO3、BaCl2、HCl及NH4NO3无标签溶液, 为鉴别它们,取四只试管分别装入一种溶液,向上述四只试管中加入少许剩下的一种溶液,下列结论错误的是( )
A.有三只试管出现沉淀时,则后加入的是AgNO3溶液
B.全部若没有什么现象变化时,后加的是NH4NO3溶液
C.一只试管出现气体,两只试管出现沉淀时,最后加入的是HCl溶液
D.若只有两只试管出现沉淀时,则最后加入的可能是BaCl2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com